Medicina intervencionista
La imagen médica, en contexto intervencionista, forma parte del proceso de acción.
En diagnóstico, la imagen soporta clasificación y decisión. En intervención, la imagen participa en el guiado, la ejecución y la verificación durante el procedimiento.
El objetivo operativo es localizar, acceder, actuar y confirmar mientras el sistema evoluciona.
La medicina intervencionista es un sistema clínico en el que imagen, geometría, decisión y ejecución operan de forma acoplada durante la acción.
1. Flujo intervencionista
El flujo operativo integra imagen, guiado, acción y verificación como etapas acopladas dentro del mismo proceso.
La imagen se integra en el proceso físico en curso, lo que exige coherencia geométrica en tiempo clínico, estabilidad del sistema durante la acción y capacidad de corrección intra-procedimiento.
2. Imagen proyectiva en intervención: C-arms y fluoroscopia
Una gran parte del intervencionismo sigue apoyándose en imagen proyectiva.
Los sistemas tipo C-arm y la fluoroscopia permiten:
- ver en tiempo casi real;
- seguir instrumentos dentro del cuerpo;
- mantener una referencia geométrica continua durante el procedimiento.
La física es conocida: proyección de rayos X, atenuación y formación de imagen. El requisito operativo es la correspondencia geométrica entre la representación y la posición del instrumento en el instante actual.
La proyección introduce ambigüedad por superposición de estructuras, pérdida de información de profundidad y dependencia del ángulo de adquisición. Y aun así, es imprescindible porque aporta continuidad temporal.
El problema geométrico del C-arm
Un C-arm no es un sistema de geometría fija. El arco puede rotar, el detector se mueve respecto al foco, y la posición del isocentro —el punto en el espacio al que convergen las distintas proyecciones— depende de la mecánica real del sistema, no de su posición nominal.
Eso significa que la correspondencia entre la imagen proyectada y el espacio físico del paciente no es trivial. Para que un instrumento visible en la imagen pueda localizarse en el espacio real con precisión suficiente, el sistema necesita:
- un modelo geométrico calibrado que relacione píxeles del detector con coordenadas del espacio;
- conocimiento de la posición real del foco y del detector para cada ángulo de adquisición;
- y la posibilidad de combinar dos proyecciones desde ángulos distintos para recuperar profundidad.
Cuando el C-arm gira, esa geometría cambia. Una calibración realizada en una posición no es necesariamente válida para otra. Los sistemas de C-arm avanzados —los llamados C-arm isocéntricos— se diseñan para que el isocentro permanezca estable durante la rotación, lo que simplifica el modelo geométrico y permite reconstrucción 3D a partir de múltiples proyecciones (C-arm con capacidad tomográfica o cone-beam CT intervencionista).
La calibración geométrica del sistema —determinar con precisión los parámetros intrínsecos y extrínsecos del modelo de proyección— es la base sobre la que se sostiene cualquier aplicación de guiado cuantitativo. Sin ella, la imagen informa cualitativamente pero no permite localizar con exactitud.
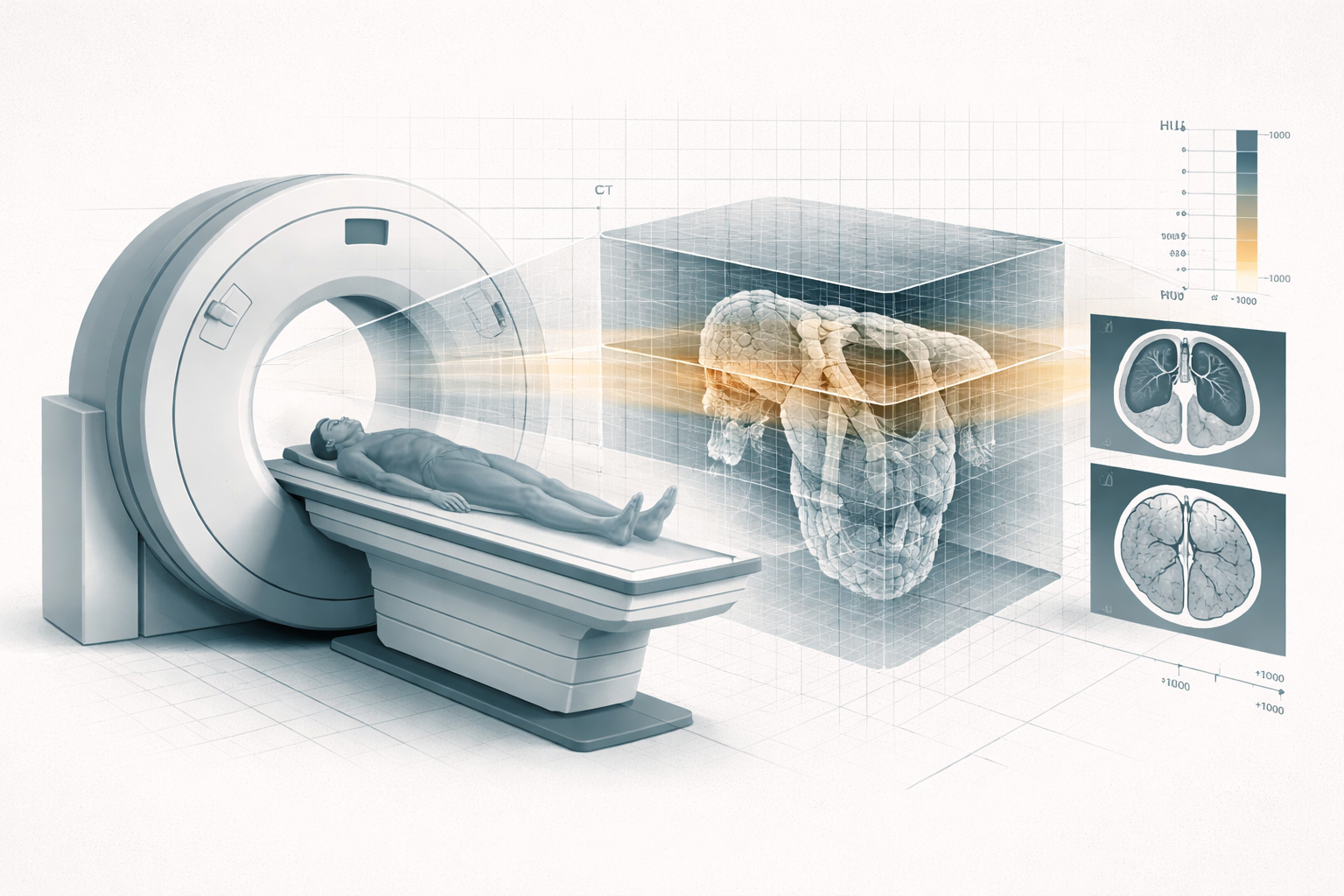
3. TAC en guiado: DRR y correspondencia imagen-realidad
El TAC reconstruye volúmenes a partir de proyecciones.
En intervención, esto permite usar:
- volúmenes preoperatorios;
- reconstrucciones;
- y DRR (Digitally Reconstructed Radiographs).
El DRR permite generar proyecciones simuladas a partir del volumen reconstruido.
Esto crea un puente entre:
- la imagen reconstruida (TAC);
- y la imagen proyectiva (fluoroscopia).
La correspondencia entre volumen reconstruido y proyección simulada depende de la posición del paciente, la coherencia geométrica, la estabilidad del sistema y el movimiento.
El problema se formula como registro entre representaciones con naturalezas físicas distintas.
Los DRR (Digitally Reconstructed Radiographs) se obtienen mediante simulación de proyección a partir del volumen TAC. Matemáticamente, implican integrar la atenuación a lo largo de trayectorias definidas por la geometría de adquisición (modelo de proyección), reproduciendo de forma sintética una radiografía equivalente.
Esto permite:
- generar vistas consistentes con el sistema de fluoroscopia;
- comparar imagen proyectiva real con una proyección calculada;
- y ajustar la geometría del sistema a una anatomía previamente conocida.
El proceso depende de:
- la calidad del volumen TAC;
- la precisión del modelo geométrico del sistema de adquisición;
- la calibración entre sistemas;
- y la estabilidad del paciente.
Desde el punto de vista físico, el DRR no añade información nueva, pero establece correspondencia entre representaciones, lo que lo convierte en un elemento clave en guiado y verificación.
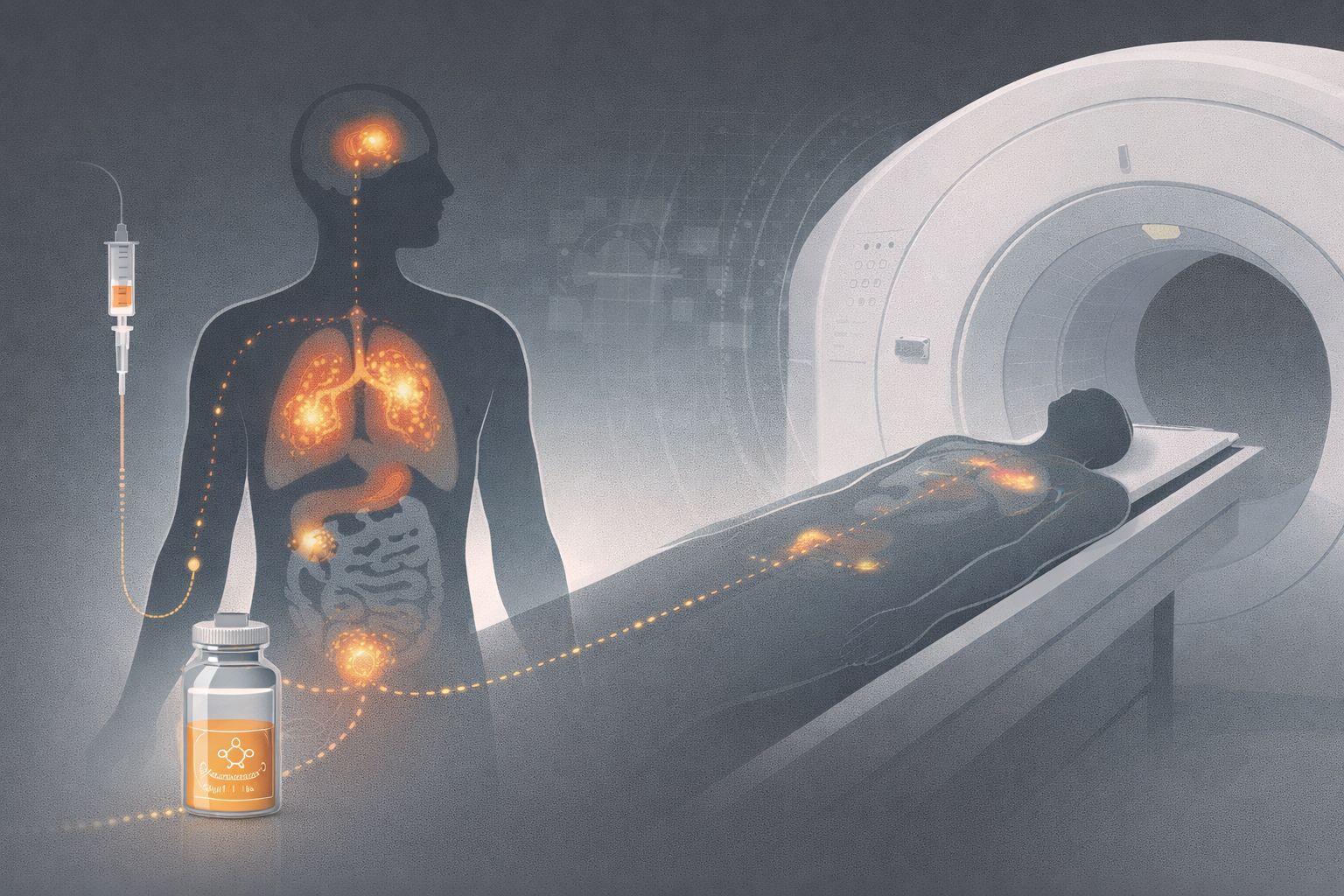
4. Cámaras gamma en intervención
Cuando se introduce detección nuclear, el problema cambia otra vez.
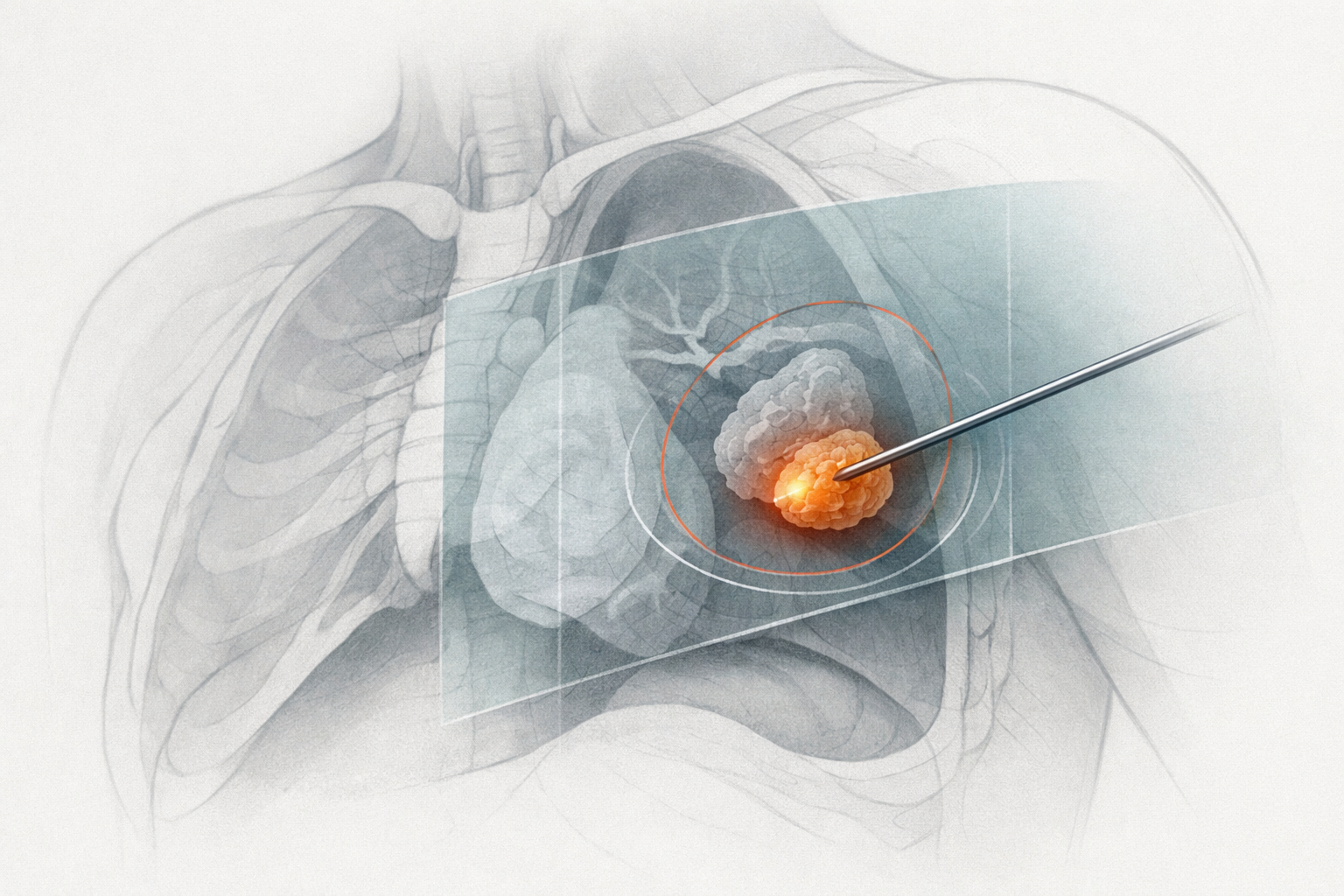
Las cámaras gamma permiten detectar actividad próxima:
- localización de tumores;
- guiado intraoperatorio;
- confirmación de resección.
Su física se basa en detección de emisión y requiere colimación para obtener información espacial.
Tipos de colimación y reconstrucción
- Colimación paralela: geometría estable, relación directa entre dirección y detección, pero con eficiencia limitada por el colimador físico.
- Colimación estenopeica (pinhole): mejora la resolución espacial en proximidad a costa de eficiencia y campo de visión.
- Cámaras Compton: eliminan el colimador físico clásico y reconstruyen la dirección de llegada de los fotones de forma estadística.
En cámaras Compton, la señal no se forma como una proyección directa. Cada interacción detectada define una superficie de probabilidad (cono de Compton) sobre la cual puede encontrarse el origen del fotón.
La imagen se obtiene mediante acumulación de múltiples eventos y resolución inversa del problema, típicamente mediante algoritmos iterativos o métodos estadísticos.
Esto introduce varias consecuencias físicas y operativas:
- La señal es intrínsecamente ruidosa, ya que cada evento contribuye de forma probabilística a la reconstrucción.
- El contraste está limitado por la dispersión de contribuciones sobre el volumen reconstruido.
- La resolución depende tanto de la estadística de eventos como de la precisión en la detección de energía y posición.
- La velocidad de adquisición y reconstrucción condiciona la viabilidad en entorno intervencionista.
A diferencia de la colimación estenopeica, donde la geometría impone una correspondencia más directa entre espacio y detección, en Compton la reconstrucción depende de la capacidad de discriminar correctamente eventos y resolver ambigüedades geométricas.
Esto exige:
- detectores con buena resolución energética y espacial;
- capacidad de distinguir coincidencias válidas;
- algoritmos robustos frente a ruido y eventos espurios;
- y una integración cuidadosa en el flujo clínico.
En contexto intervencionista, el interés de estas cámaras reside en su potencial para proporcionar información funcional sin necesidad de colimadores restrictivos, pero a costa de un problema inverso más complejo.
La discusión no es únicamente tecnológica. Es también metodológica: cómo validar, cómo interpretar señal con bajo contraste y cómo integrar esta información en decisiones clínicas en tiempo limitado.
Desde el punto de vista organizativo, la incorporación de técnicas basadas en detección nuclear requiere un entorno hospitalario específico. No se trata únicamente de disponer del detector, sino de integrar un servicio de medicina nuclear completo: gestión de radiofármacos, protección radiológica, procedimientos autorizados y registro de la instalación ante el regulador (CSN).
Esto introduce una dependencia estructural: la viabilidad de la tecnología no está determinada únicamente por su rendimiento físico, sino por la capacidad del sistema sanitario para sostenerla. Para el profesional, esto implica situar cada técnica dentro de un contexto real de recursos, integración y soporte clínico.
–
5. El problema real: no hay tiempo real
Las técnicas disponibles presentan latencias de adquisición, integración y reconstrucción que limitan la correspondencia instantánea entre imagen y estado físico.
Durante el procedimiento, el sistema cambia por respiración, movimiento de órganos y efecto de la propia intervención.
La representación no coincide necesariamente con el estado actual, lo que introduce error de guiado dependiente del tiempo.
6. Validación clínica y operativa
La validación requiere demostrar mejora en localización efectiva, resultado clínico, riesgo o eficiencia. El impacto depende del operador, el contexto clínico, la selección de pacientes y la integración en el sistema.
Pero antes de la validación clínica existe una cadena de verificación técnica que con frecuencia se omite o se abrevia: la demostración de que el sistema hace lo que dice hacer desde el punto de vista geométrico y dosimétrico.
Controles técnicos previos a la validación clínica
Un sistema de guiado intervencionista debe pasar por varias capas de verificación antes de que tenga sentido evaluar su impacto clínico:
Verificación geométrica: comprobar que la correspondencia entre imagen y espacio físico está dentro de los límites de exactitud especificados. Esto implica usar fantomas geométricos —objetos de geometría conocida con marcadores localizables en imagen— para medir el error de proyección, el error de localización en profundidad y la estabilidad del modelo con la posición del arco.
Verificación dosimétrica: en sistemas con RX, comprobar que la dosis al paciente y al personal es consistente con los protocolos y que los sistemas de control de dosis funcionan correctamente.
Verificación de registro: cuando el sistema combina imagen preoperatoria (TAC, RM) con imagen intraoperatoria, verificar que el registro entre ambas representaciones introduce un error dentro de los márgenes clínicamente aceptables para la indicación.
Tests de aceptación y repetibilidad: demostrar que el sistema produce resultados consistentes entre sesiones, entre operadores y entre unidades del mismo modelo si se trata de un dispositivo comercializado.
Solo cuando esa base técnica está establecida tiene sentido diseñar un estudio de validación clínica que evalúe impacto en el resultado del procedimiento.
7. Escalas reales: del robot al dentista
El intervencionismo ocurre en múltiples escalas:
- quirófanos altamente tecnificados;
- sistemas robóticos;
- unidades clínicas intermedias;
- consultas donde no hay físicos médicos.
La física médica se implementa en entornos con niveles heterogéneos de control, calidad de imagen y capacidad de validación, lo que condiciona el riesgo operativo.
8. Radioterapia coadyuvante intraoperatoria
En algunos contextos, la intervención también incluye tratamiento.
La radioterapia intraoperatoria integra adquisición, decisión y tratamiento en un único acto clínico, lo que introduce requisitos estrictos de coherencia geométrica y dosimétrica.
A diferencia de la planificación radioterápica convencional, donde se parte de imágenes preoperatorias estables y bien caracterizadas, en este contexto la definición de volúmenes y condiciones dosimétricas se realiza sobre información intraoperatoria, incompleta y dinámica. Los sistemas de planificación no operan sobre una geometría fija, sino sobre una situación clínica en evolución.
El ciclo operativo integra localización, intervención, tratamiento y verificación en tiempo clínico.
Esto implica:
- definir volúmenes tratables en un entorno dinámico;
- establecer relaciones espaciales con órganos de riesgo durante la intervención;
- adaptar la dosimetría a condiciones no completamente reproducibles;
- y verificar la entrega en condiciones clínicas reales.
A diferencia de la radioterapia convencional, donde existe separación entre planificación y entrega, en este contexto ambas fases se acoplan, lo que reduce margen de corrección y aumenta la exigencia de validación intra-procedimiento.
La integración de imagen en este entorno no es únicamente informativa, sino estructural: condiciona directamente la decisión terapéutica.
9. Línea de investigación: cámaras gamma, guiado y calibración multimodal
Las cámaras gamma representan una línea especialmente interesante en este contexto. Permiten localizar actividad en proximidad, asistir sistemas de guiado, confirmar resecciones y explorar nuevas formas de interacción entre imagen funcional y acción quirúrgica.
Su desarrollo implica optimización de colimación, mejora de reconstrucción, integración en flujos clínicos y validación en escenarios reales. Pero hay una dimensión que con frecuencia queda en segundo plano en la literatura: cómo se calibra el sistema y cómo se verifica que la localización que proporciona es exacta.
Una cámara gamma intervencionista no funciona sola. Su información es útil solo cuando puede relacionarse con el espacio físico del procedimiento: la posición de la mano del cirujano, la geometría del campo quirúrgico, la relación con la imagen de fluoroscopía o con el volumen TAC preoperatorio. Establecer esa correspondencia requiere calibración espacial del sistema en el entorno real de uso.
Esa misma lógica se extiende a los sistemas que combinan imagen de rayos X con sensores ópticos —cámaras RGB o RGB-D— para recuperar información tridimensional a partir de proyecciones. La calibración conjunta de ambos sistemas, la caracterización de su geometría relativa y la validación de la exactitud de localización 3D son problemas abiertos con aplicación directa en guiado intervencionista.
Calibración y verificación de sistemas de imagen para guiado Modelos geométricos, fantomas, calibración conjunta RX-óptica, controles numéricos y evaluación de exactitud en sistemas de guiado intervencionista.10. Resumen
La medicina intervencionista es un sistema en el que la imagen guía la acción bajo incertidumbre geométrica y temporal.
El rendimiento depende de la correspondencia entre representación e intervención, de la gestión del movimiento y de la capacidad de validación intra-procedimiento.