El PET
El PET (positron emission tomography, tomografía por emisión de positrones) ocupa una posición específica dentro de la imagen médica. Su lógica no parte del contraste anatómico primario, sino de una pregunta funcional: qué actividad biológica está mostrando ese tejido.
Por eso el PET es, ante todo, una técnica de imagen funcional. Y también por eso obliga a abrir una puerta que hasta ahora apenas habíamos rozado en esta serie: la de la medicina nuclear.
En la práctica clínica, el PET se asocia sobre todo a imagen metabólica como una de las formas más importantes de imagen funcional. No toda imagen funcional es metabólica, pero en PET la dimensión metabólica ha sido históricamente central.
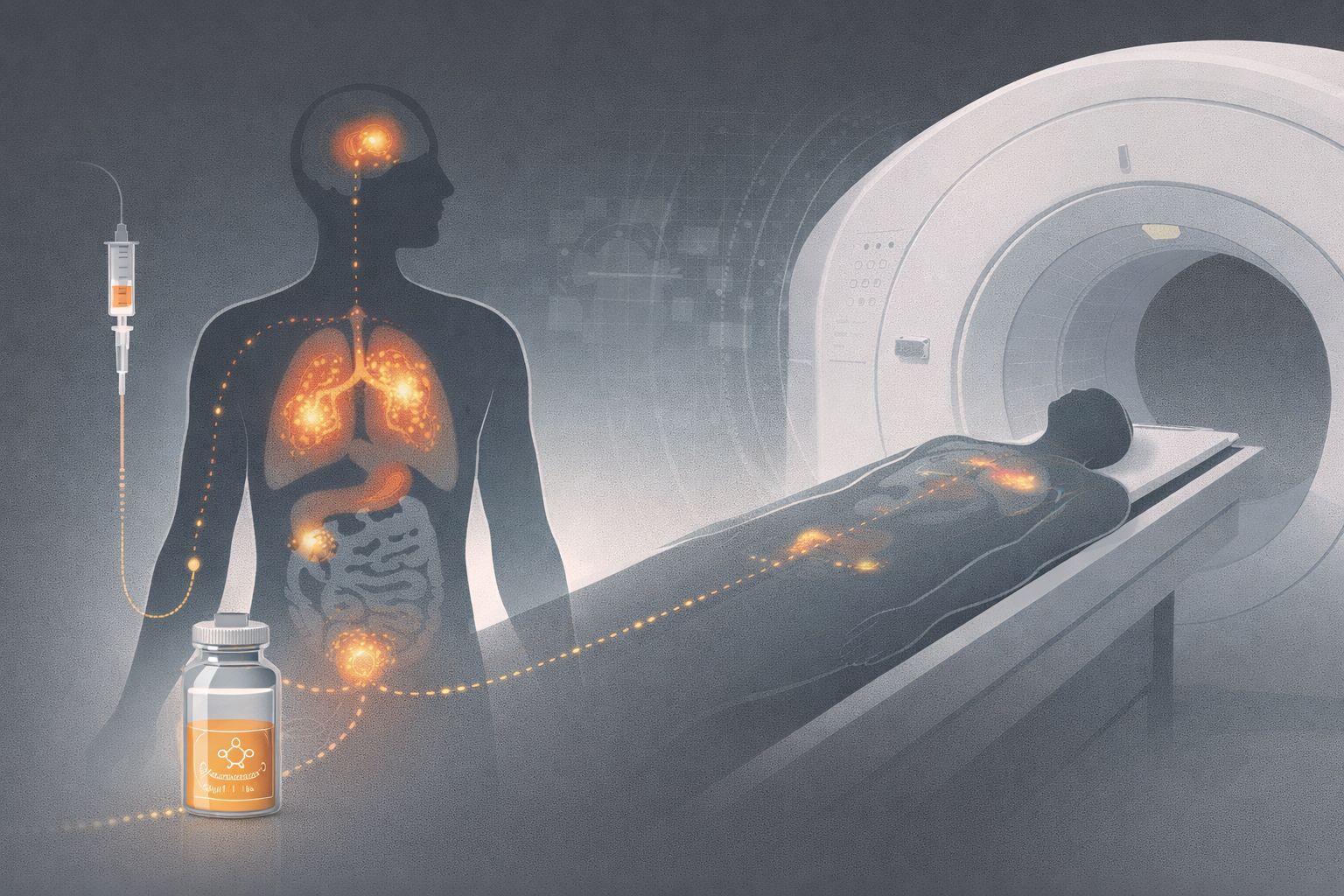
No hace falta convertir el blog en un tratado completo de medicina nuclear para entender su importancia. Basta con dejar clara una idea. El PET no construye imagen porque un haz externo atraviese el cuerpo ni porque un tejido genere señal bajo un campo magnético. Construye imagen porque se administra un radiofármaco que participa, se distribuye o se fija según una lógica biológica determinada, y luego el sistema detecta esa actividad desde dentro.
1. Historia y desarrollo instrumental
Como en las otras modalidades, aquí también conviene citar a la gente que convirtió una buena idea física en una herramienta clínica real. El PET moderno suele asociarse sobre todo a Michel Ter-Pogossian, Edward Hoffman y Michael Phelps, y también a nombres como Henry Huang y Nizar Mullani en el desarrollo instrumental de los primeros sistemas modernos. Su trabajo en los años setenta fue decisivo para pasar de la detección de positrones como posibilidad experimental a escáneres tomográficos útiles en clínica e investigación.
La historia importa porque explica algo esencial: el PET no nació solo de la medicina nuclear clásica, sino de la combinación entre radioquímica, instrumentación de detectores, coincidencias electrónicas y reconstrucción matemática. En ese sentido se parece bastante al TAC: no basta con tener un fenómeno físico interesante. Hace falta una arquitectura instrumental capaz de explotarlo.
Y esa arquitectura llevó al PET a una escala nueva. La medicina nuclear dejaba de ser solo imagen planar de captación para convertirse en tomografía funcional, es decir, en volumen reconstruido a partir de eventos detectados en coincidencia.
2. Tomografía nuclear
El PET pertenece a la medicina nuclear, pero conviene distinguirlo bien de la imagen gammagráfica plana o incluso de otras modalidades nucleares más clásicas. No estamos ante una “placa radiactiva”. Estamos ante una técnica tomográfica.
Eso significa que el PET reconstruye volumen. No da solo una proyección; da una distribución tridimensional de actividad. Y eso cambia muchísimo su utilidad.
Lo que se detecta no es un contraste anatómico primario, sino la emisión asociada al radionúclido incorporado al radiofármaco. En PET, el positrón emitido acaba aniquilándose con un electrón y produciendo dos fotones detectables en coincidencia. A partir de muchísimos eventos así, el sistema reconstruye la distribución espacial del trazador.
La técnica, por tanto, es nuclear y funcional, pero no por ello vaga o difusa en sentido geométrico. Un buen PET es una imagen tomográfica precisa, aunque su resolución y su tipo de información sean muy distintos de los de un TAC o una RM.
3. Radiofármaco y diana biológica
La máquina importa, claro. Pero en PET el verdadero protagonista conceptual es el radiofármaco.
Y aquí merece la pena cambiar un poco el lenguaje mental. No se trata solo de “inyectar un isótopo”. Se administra un medicamento radiológico o radiofármaco, es decir, una molécula portadora con interés biológico unida a un radionúclido emisor de positrones. La utilidad clínica no la define solo la física del detector. La define también qué molécula se usa, qué vía metabólica sigue, dónde se fija, cómo se elimina y cuál es la vida media del isótopo.
Eso obliga a tratar simultáneamente imagen, farmacología, biología tumoral y física del detector.
Entre los trazadores más conocidos están:
- FDG (fludeoxiglucosa F-18), muy ligada al metabolismo glucídico y central en oncología;
- NaF F-18, útil en imagen ósea;
- ammonia N-13, en perfusión miocárdica;
- y una familia creciente de trazadores más específicos, por ejemplo en próstata, sistema nervioso o receptores concretos.
Eso hace que el PET no sea “una sola técnica con una sola indicación”. Sea una plataforma funcional cuya pregunta clínica cambia con el trazador.
4. Vida media, actividad y logística
En PET la dosis no depende solo de cuánta actividad se administra, sino también de la vida media del radionúclido, de la distribución biológica del radiofármaco, del tiempo entre producción, administración y adquisición, y de la forma en que el trazador se elimina.
Aquí la física temporal importa mucho. Algunos radionúclidos tienen vidas medias muy cortas y exigen una logística extremadamente ajustada. Otros, como el F-18, permiten una operativa más cómoda y por eso han tenido tanta expansión clínica.
La vida media condiciona varias cosas a la vez:
- la ventana de producción y transporte;
- la organización del servicio;
- la actividad disponible en el momento de inyección;
- la dosis absorbida por el paciente;
- y el diseño completo del flujo asistencial.
Eso vuelve al PET una modalidad muy hospitalaria en el sentido fuerte de la palabra. No basta con tener el escáner. Hace falta una cadena de producción, dispensación, control, administración y adquisición extremadamente bien coordinada.
5. Cristales centelleadores y detectores
El PET tampoco se entiende bien si uno no mira sus detectores. Aquí el protagonista instrumental clásico es el cristal centelleador. Los fotones de 511 keV deben ser detenidos con buena eficiencia y convertir esa interacción en luz detectable. Y de esa cadena dependen sensibilidad, resolución, capacidad de cuantificación y, cada vez más, la precisión temporal del sistema.
Históricamente hubo distintos materiales, pero en la práctica clínica moderna el protagonismo ha pasado por cristales como:
- BGO (
bismuth germanate), muy importante durante mucho tiempo en PET corporal; - LSO (
lutetium oxyorthosilicate) y LYSO (lutetium yttrium oxyorthosilicate), que han ganado muchísimo terreno por su combinación de poder de frenado, rendimiento lumínico y respuesta temporal; - y otras variantes lutecio-basadas o diseños más específicos según aplicación.
La elección del cristal no es un detalle menor. Afecta a:
- la probabilidad de interacción de los fotones de 511 keV;
- la cantidad de luz generada;
- la velocidad con la que esa luz aparece y decae;
- la resolución energética;
- y la posibilidad real de hacer PET con buen
TOF(time-of-flight, tiempo de vuelo).
Durante muchos años la lectura se hizo sobre todo con fotomultiplicadores (PMT, photomultiplier tubes). Hoy gran parte del salto tecnológico viene de los SiPM (silicon photomultipliers), que permiten detectores más compactos, mejor comportamiento temporal, integración más moderna de electrónica y compatibilidad con sistemas híbridos como PET-RM (PET combinado con resonancia magnética). En otras palabras: el PET actual no es solo mejor porque haya mejores reconstrucciones. También es mejor porque el detector ha cambiado mucho.
6. Tiempo de vuelo (TOF)
El time-of-flight, o TOF (tiempo de vuelo), ha sido una de las líneas instrumentales más importantes del PET.
Si detectamos los dos fotones de aniquilación y además medimos con suficiente precisión la diferencia temporal entre su llegada a detectores opuestos, no solo sabemos que el evento ocurrió en una determinada línea de respuesta. También podemos estimar mejor en qué zona de esa línea tuvo lugar.
Eso no resuelve la reconstrucción por arte de magia, pero sí reduce incertidumbre estadística y mejora la relación señal-ruido. En la práctica clínica, un buen TOF ayuda a obtener imágenes más limpias, reconstrucciones más robustas y, en algunos escenarios, mejores tiempos de adquisición o mejor comportamiento en pacientes difíciles.
Durante décadas fue una promesa muy atractiva pero tecnológicamente dura de cumplir. Hacían falta cristales rápidos, mucha luz, detectores con gran precisión temporal y electrónica capaz de leer todo eso sin perder el control del sistema. Por eso el TOF ha ido entrando de verdad en clínica a medida que mejoraban los centelleadores, los fotodetectores y la electrónica asociada.
En términos prácticos, el TOF convierte mejor información temporal en mejor localización estadística de los eventos. No sustituye la reconstrucción tomográfica, pero mejora su comportamiento.
7. Captación e indicaciones clínicas
La fortaleza del PET está en que puede mostrar actividad biológica de forma muy sensible. Esa es la razón por la que su gran territorio clásico ha sido la oncología.
En cáncer, el PET ayuda a:
- detectar enfermedad metabólicamente activa;
- valorar extensión;
- diferenciar mejor ciertos territorios anatómicos dudosos;
- detectar recaída;
- apoyar estadificación;
- monitorizar respuesta al tratamiento;
- y en algunos contextos seleccionar mejor qué zonas merecen especial atención terapéutica o diagnóstica.
En términos clínicos, el PET no destaca por representación anatómica, sino por resaltar qué tejido se está comportando de manera anómala.
Y aunque oncología sea el gran caso, no es el único. También tiene papeles importantes en:
- neurología, por ejemplo en metabolismo cerebral o en ciertos trazadores dirigidos;
- cardiología, en perfusión y viabilidad miocárdica;
- y en campos cada vez más especializados donde el trazador abre preguntas más finas que las puramente anatómicas.
8. Significado clínico de la imagen funcional
Decir que el PET es funcional no significa que sea mágico. Significa que la imagen representa una distribución biológica mediada por un radiofármaco, no solo la forma del órgano.
Eso tiene dos consecuencias enormes.
La primera: puede detectar alteraciones antes de que la anatomía se deforme de forma llamativa.
La segunda: obliga a interpretar siempre la captación dentro de un contexto clínico y biológico. Una captación aumentada no es automáticamente “cáncer”, del mismo modo que una ausencia de captación llamativa no agota por sí sola toda la interpretación. Inflamación, infección, metabolismo normal de ciertos órganos, fisiología del trazador y preparación del paciente modifican el mapa que luego vemos.
Aquí aparece uno de los grandes aprendizajes del PET: la imagen funcional es potentísima, pero nunca debe leerse como si fuese un color automático de verdad definitiva.
9. Eliminación del trazador
Una parte muy importante del PET no está solo en dónde se fija el trazador, sino también en cómo se elimina.
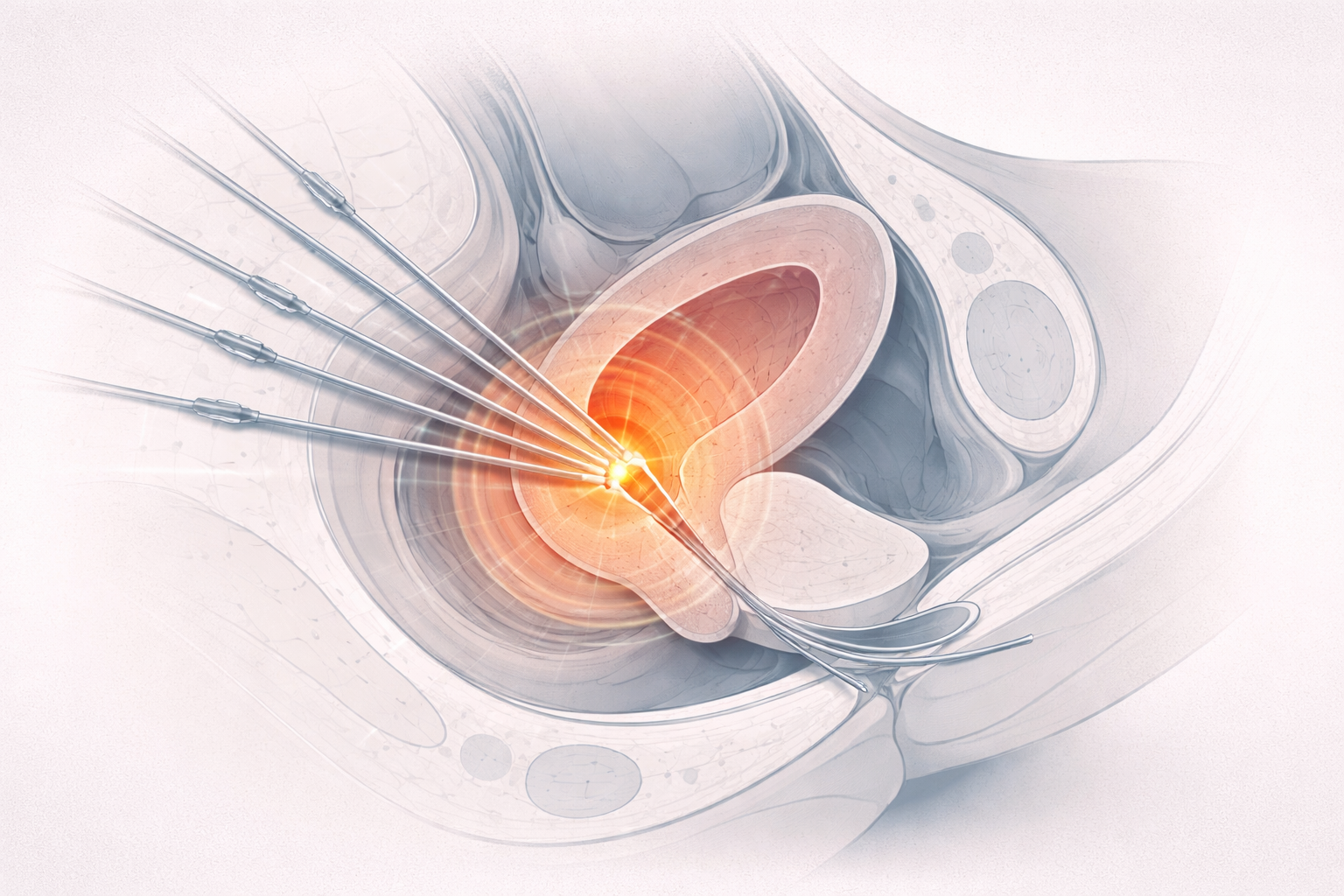
En muchos radiofármacos, y de forma muy conocida con FDG, la eliminación renal y urinaria tiene un papel importante. Eso significa que la actividad puede acumularse en riñones, uréteres y vejiga. Desde el punto de vista de la física y de la dosimetría esto importa, pero desde el punto de vista clínico importa todavía más cuando la región de interés está cerca.
En pelvis, por ejemplo, la actividad urinaria puede complicar la lectura de estructuras vecinas. Por eso en determinados protocolos se cuidan especialmente la hidratación, el vaciado vesical y, en algunos contextos concretos, incluso el sondaje urinario para reducir actividad cercana cuando la indicación lo justifica. No es una regla universal para todos los PET, pero sí una muestra muy buena de cómo la fisiología de eliminación condiciona la utilidad real de la prueba.
Ese detalle encaja muy bien con lo que querías señalar en próstata: a veces la pregunta clínica no depende solo del tumor y del trazador, sino también de cómo el propio cuerpo decide expulsar el fármaco.
10. Cuantificación y límites
El PET tiene una enorme sensibilidad, pero eso no significa que no tenga problemas de cuantificación o de interpretación.
Su resolución anatómica es más limitada que la del TAC o la RM. La corrección de atenuación importa mucho. El movimiento afecta. El ruido afecta. Los volúmenes pequeños sufren efectos parciales. La cuantificación, por ejemplo mediante medidas como el SUV (standardized uptake value), es útil, pero no debe tratarse como si cada número fuese una verdad aislada del protocolo, del tiempo postinyección, del equipo y del contexto clínico.
Aquí se ve de nuevo la filosofía general de la física médica: una medida cuantitativa puede ser muy valiosa sin convertirse por ello en una magnitud absoluta fuera del sistema que la produce.
11. Integración con otras modalidades
Aunque el PET sea muy potente, rara vez se queda solo. Y eso también dice algo importante sobre su naturaleza.
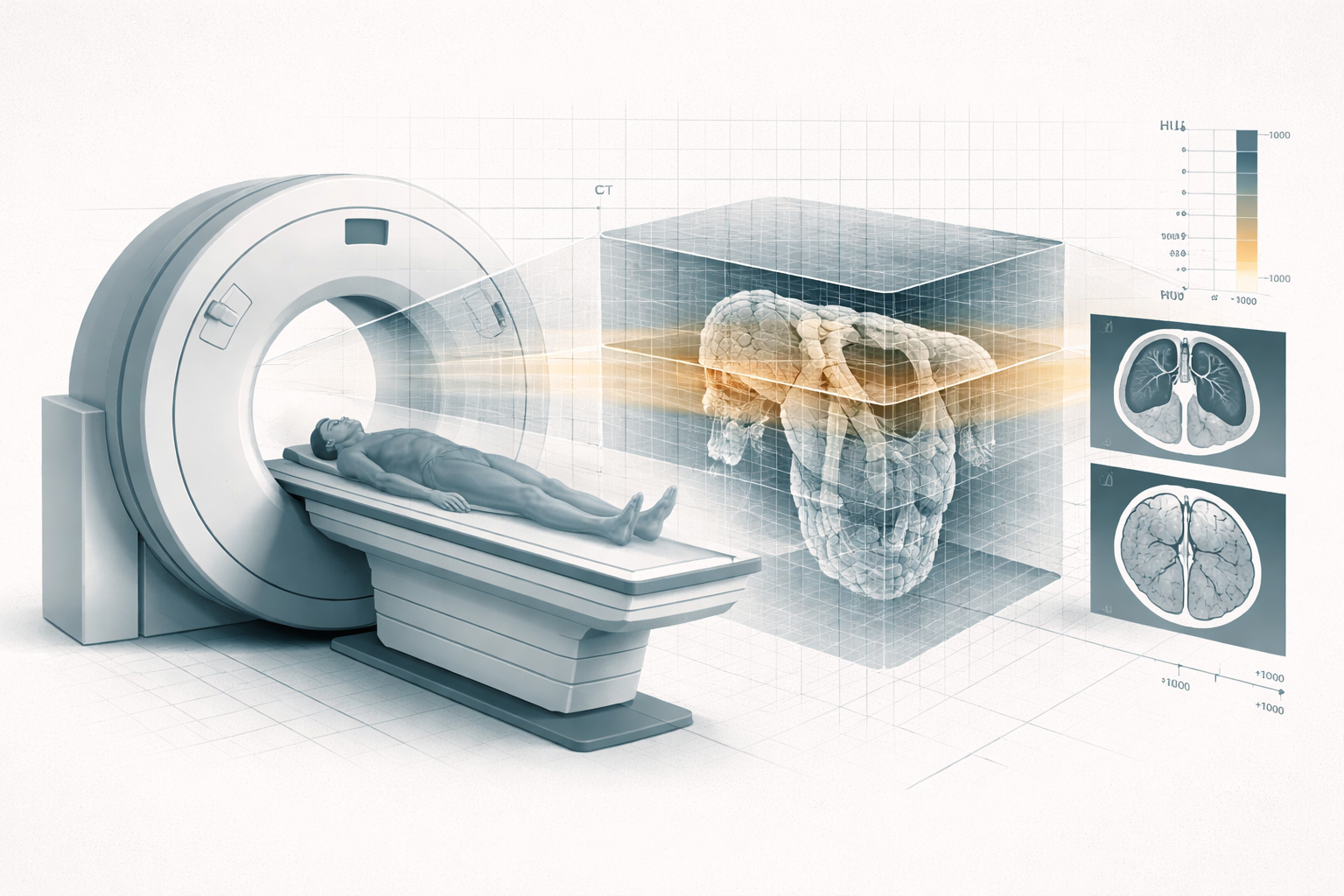
El PET necesita, muchas veces, una anatomía que lo acompañe. De ahí el enorme éxito del PET-TAC (PET combinado con tomografía computarizada), donde la información funcional del trazador se superpone o se registra con la anatomía y la corrección de atenuación del TAC. Esa alianza ha sido decisiva clínicamente.
Más adelante tendrá sentido dedicar una pieza propia a PET-TAC e imagen molecular. Pero incluso aquí ya conviene dejar la intuición correcta: el PET no pierde identidad cuando se fusiona con otras modalidades. La gana. Porque su fuerza no está en competir anatómicamente con el TAC, sino en añadir una capa funcional que el TAC por sí solo no puede dar.
12. PET e imagen molecular
El PET además abre una idea todavía más amplia: la de imagen molecular.
No se trata solo de ver dónde está una lesión. Se trata de ver qué expresa, qué consume, qué receptor presenta, qué vía metabólica sigue o qué comportamiento biológico sugiere. Eso lo acerca mucho a la oncología de precisión y a una medicina menos basada en siluetas anatómicas y más basada en funciones y dianas.
Por eso, aunque la medicina nuclear no vaya a ser el gran leitmotiv de esta serie, sería un error dejar al PET como una simple rareza lateral. Tiene un papel muy serio porque representa una transición importante: pasar de la anatomía a la biología visible.
13. Indicaciones y límites
El PET es una modalidad extraordinaria, pero no universal. No reemplaza a TAC, RM o ultrasonidos. No responde bien a todas las preguntas. No todos los tejidos ni todas las enfermedades tienen un trazador igual de útil. No todos los incrementos de captación significan lo mismo. Y no toda indicación justifica su coste, su logística y su dosis.
Pero precisamente por eso resulta tan interesante.
Porque obliga a pensar la imagen médica desde la función y no solo desde la forma. Su papel técnico consiste en convertir la medicina nuclear en una modalidad tomográfica funcional con utilidad clínica alta.
Relacionado
Para ampliar
- RadiologyInfo - PET/CT
- NIBIB - Nuclear Medicine Fact Sheet
- FDA - PET Drug SPL
- FDA - Oversight of PET Drug Products
- Journal of Nuclear Medicine - One Hundred Years of the Tracer Principle
- Journal of Nuclear Medicine - Advances in Detector Instrumentation for PET
- PMC - Update on latest advances in Time-Of-Flight PET
- Journal of Nuclear Medicine - A Conversation Between Michael Phelps and Jason Lewis
- IAEA - Nuclear Medicine Equipment
- NIBIB - Nuclear Medicine