La mamografía
La mamografía es una técnica radiográfica especializada cuya relevancia no depende solo del equipo o de la física de adquisición. Su papel clínico y sanitario viene definido por su integración en programas de cribado, circuitos diagnósticos y decisiones organizativas de gran escala.
La mamografía no es solo una técnica de rayos X aplicada a una anatomía concreta. También implica invitación poblacional, lectura radiológica, recall, derivación diagnóstica, biopsia, gestión de incertidumbre, control de calidad, epidemiología y asignación de recursos. En física médica, esto significa trabajar con una técnica de imagen que funciona dentro de un sistema sanitario completo.
1. Una técnica, pero también un programa
La mamografía es probablemente la técnica de screening o cribado más conocida en práctica clínica y salud pública. Reúne varias cosas difíciles de conseguir a la vez:
- una base física suficientemente madura;
- un coste relativamente bajo comparado con otras técnicas avanzadas;
- una disponibilidad amplia;
- capacidad para detectar hallazgos antes de que sean palpables;
- y posibilidad real de desplegarse a escala poblacional.
Su análisis requiere considerar tanto la imagen como el programa de salud pública en el que se integra.
Y ahí conviene recordar algo básico: una prueba de screening no se justifica solo porque sea técnicamente brillante. En la tradición clásica de criterios de cribado recogida por la OMS — los principios de Wilson y Jungner (1968), que siguen siendo la referencia conceptual más citada en salud pública — la prueba es solo una de las condiciones necesarias, no la suficiente. También tiene que ser aceptable para la población, tener detrás un circuito diagnóstico y terapéutico realista, y sostenerse con un coste y una organización razonables.
Cuando una técnica se incorpora a cribado, su rendimiento pasa a depender también de capas organizativas adicionales:
- a quién se invita,
- con qué periodicidad,
- cómo se comunica,
- cuántos equipos hay,
- cuántos radiólogos leen,
- qué se considera positivo,
- cómo se maneja el recall,
- y qué pasa después del hallazgo.
Ahí la mamografía deja de ser solo física del contraste y se convierte también en planificación.
2. Principios de cribado: Wilson y Jungner
En 1968, la OMS publicó el documento Principles and Practice of Screening for Disease, de Wilson y Jungner. Su objetivo era establecer qué condiciones debe cumplir una enfermedad y un programa sanitario antes de que tenga sentido desplegar una prueba de cribado. No todas las enfermedades merecen cribado, y no todas las pruebas técnicamente capaces de detectar algo justifican un programa poblacional.
Los criterios que propusieron, simplificados, son estos:
- la enfermedad debe ser un problema sanitario importante;
- debe existir un tratamiento aceptado y eficaz para los casos identificados;
- deben estar disponibles los recursos para diagnóstico y tratamiento;
- debe existir una fase latente o sintomática precoz reconocible;
- debe haber una prueba o exploración adecuada para detectarla;
- la prueba debe ser aceptable para la población;
- la historia natural de la enfermedad debe estar suficientemente comprendida;
- debe existir una política acordada sobre a quién tratar;
- el coste del programa debe estar equilibrado con el beneficio esperado;
- y el cribado debe ser un proceso continuo, no una acción puntual.
La mamografía cumple muchos de estos criterios para el cáncer de mama en grupos etarios definidos. Pero no todos por igual, y no en todas las poblaciones del mismo modo. Esa lectura cuidadosa es lo que distingue una política de cribado seria de una decisión de intuición tecnológica.
3. Información que aporta la prueba
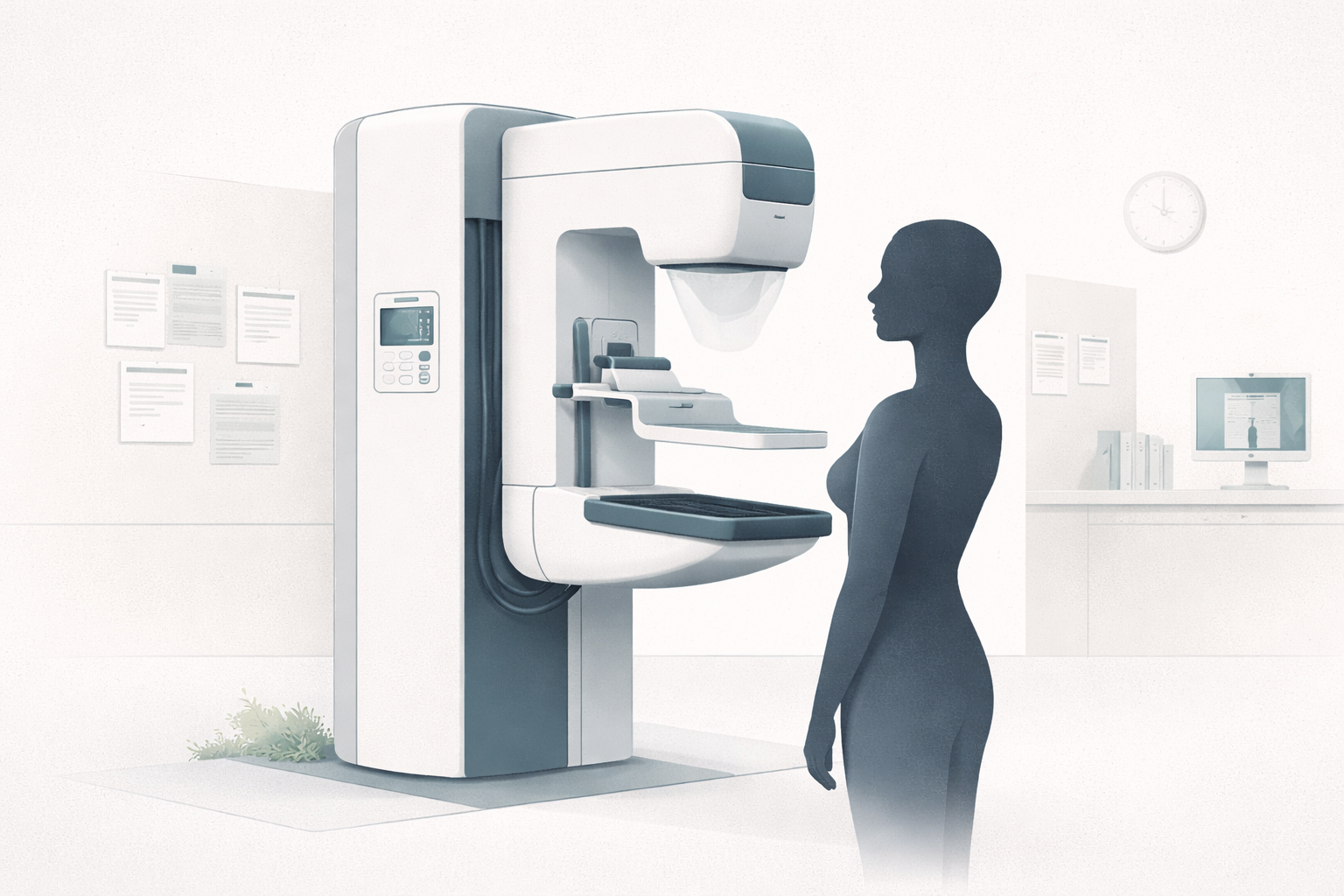
Desde el punto de vista de la imagen, la mamografía es una radiografía especializada de mama, optimizada para una anatomía, un rango de energías, una compresión y una calidad de imagen muy particulares. No busca exactamente lo mismo que una radiografía convencional de tórax o hueso. Busca sacar rendimiento a contrastes sutiles, microcalcificaciones, masas, distorsiones arquitecturales y asimetrías en un tejido donde la lectura exige mucho más que detectar una estructura muy blanca o muy negra.
Lo que la prueba aporta no es un diagnóstico cerrado por sí solo, sino una señal útil de sospecha o de tranquilidad relativa. Puede:
- detectar lesiones pequeñas aún no palpables;
- mostrar microcalcificaciones sospechosas;
- revelar distorsiones o asimetrías;
- establecer una línea basal;
- comparar con estudios previos;
- y decidir si hace falta ampliar con tomosíntesis, ecografía, resonancia o biopsia.
Su función clínica es ordenar el siguiente paso diagnóstico correcto, no cerrar por sí sola todo el proceso.
4. Signo radiológico, sospecha y patología
Uno de los errores conceptuales más frecuentes al hablar de mamografía es confundir lo que la prueba detecta con lo que la prueba diagnostica.
La mamografía detecta signos: densidades, microcalcificaciones, distorsiones arquitecturales, asimetrías. Esos signos son observaciones físicas en la imagen. No son cáncer. Pueden estar asociados con cáncer, pueden ser compatibles con cáncer, pueden elevar la probabilidad de que haya un proceso maligno subyacente. Pero no son el diagnóstico.
El diagnóstico de cáncer de mama es histológico. Lo da la anatomía patológica tras biopsia, no la mamografía.
Esta distinción no es un tecnicismo menor. Tiene consecuencias directas:
- una mamografía positiva no significa que la paciente tenga cáncer;
- una mamografía negativa no garantiza que no lo tenga;
- la cadena entre signo radiológico y diagnóstico pasa por recall, imagen adicional, biopsia e histología;
- y la gravedad del signo es una estimación probabilística, no una certeza.
Los sistemas de clasificación como BI-RADS (Breast Imaging Reporting and Data System) formalizan exactamente eso: asignan categorías que expresan la probabilidad de malignidad según los hallazgos, y recomiendan la acción siguiente. No son diagnósticos. Son estimaciones de riesgo que orientan el manejo.
5. Tomosíntesis: más proyecciones, no exactamente un TAC
Aquí merece aparecer una técnica que ha cambiado bastante el paisaje reciente de la mamografía: la tomosíntesis mamaria digital.
La idea física resulta muy reconocible para cualquiera que venga de la imagen con rayos X. En lugar de una sola proyección, el tubo adquiere múltiples imágenes desde distintos ángulos sobre un arco limitado. Luego un algoritmo reconstruye un conjunto de cortes finos o “capas” del volumen mamario. Eso reduce el problema clásico del solapamiento tisular y mejora la lectura en muchos casos, especialmente cuando la superposición de estructuras complica la mamografía digital convencional.
Se parece, por tanto, a una forma de tomografía. Pero conviene no pasarse con la analogía. La tomosíntesis no es un TAC de mama en sentido pleno:
- trabaja con un ángulo limitado, no con una cobertura tomográfica completa;
- mejora la separación entre planos, pero no reconstruye un volumen con la robustez geométrica de un TAC convencional;
- y, sobre todo, no produce una cuantificación equivalente a la del TAC, donde cada vóxel puede asociarse a un número Hounsfield.
Dicho de otra forma: la tomosíntesis añade profundidad útil a una técnica de proyección, pero no la convierte en una tomografía cuantitativa completa.
Clínicamente esto importa porque mejora detección y lectura en determinados escenarios sin romper del todo la lógica organizativa de la mamografía. La FDA reconoce la digital breast tomosynthesis (DBT) como modalidad de mamografía, y el NCI la describe precisamente como una técnica que adquiere múltiples imágenes desde distintos ángulos para reconstruir una serie de “slices” del tejido mamario. Es decir, un paso adelante muy serio, pero dentro de la familia de la mamografía, no fuera de ella.
4. Papel de la mamografía en cribado
Hay motivos técnicos, pero también motivos de sistema.
La mamografía ha logrado una posición muy fuerte porque ofrece una combinación poco frecuente:
- coste contenido;
- estandarización razonable;
- capacidad de despliegue;
- beneficio poblacional plausible;
- y una cadena de trabajo que puede integrarse en servicios de radiología y programas públicos de cribado.
En términos de planificación sanitaria, puede leerse como una intervención situada en la base de la pirámide de Kaiser: una herramienta relativamente barata, reproducible y escalable, pensada para llegar a mucha población antes de fases más costosas y complejas de la enfermedad.
Por eso la mamografía nunca debería leerse solo como una imagen de mama. Es una pieza de gestión poblacional del riesgo.
5. Mortalidad, supervivencia y límites de interpretación
Decir que la mamografía ha sido un éxito necesita un poco de precisión para no convertir la frase en propaganda.
Lo más sólido es esto: la mamografía es la modalidad de cribado mamario más extendida y existe evidencia de que reduce la mortalidad específica por cáncer de mama en ciertos grupos etarios, especialmente en mujeres entre 50 y 69 años, aunque el tamaño exacto del beneficio y su balance con los daños sigue siendo objeto de discusión técnica y metodológica. El resumen PDQ del NCI sigue siendo especialmente útil aquí porque no solo enumera beneficios, también pone delante los falsos positivos, el sobrediagnóstico y la complejidad de interpretar los resultados a largo plazo.
Aquí conviene hacer una distinción importante. Para juzgar el cribado, la mortalidad es una medida más limpia que la supervivencia a 5 años, porque la supervivencia puede verse inflada por adelanto diagnóstico, sesgos de selección o cambios de estadio sin que todo ese efecto se traduzca del mismo modo en vidas salvadas. Aun así, la supervivencia sigue siendo clínicamente informativa cuando se interpreta con cuidado.
Los datos de SEER son muy elocuentes como contexto:
- la supervivencia relativa a 5 años para cáncer de mama femenino es del 91,7% en el conjunto actual publicado;
- cuando el diagnóstico es localizado, la supervivencia relativa a 5 años es del 100,0% en la tabla vigente de SEER.
Eso no significa que “la mamografía garantice” esos resultados. Significa algo más serio y más útil: detectar antes suele desplazar casos hacia estadios donde el pronóstico es mucho mejor y las opciones terapéuticas son menos devastadoras. La relación exacta entre cribado, tratamiento y supervivencia merece un análisis propio, y de hecho lo tendrá mejor en una pieza dedicada a esperanza de vida y cáncer. Pero para este artículo basta con una idea limpia: la mamografía forma parte de la infraestructura que permite llegar antes.
6. Aceptación, participación y tolerancia
Una técnica de screening vale lo que valga su aceptación real. Y la aceptación no es solo una cuestión de comunicación o de campaña sanitaria: es una variable que puede hacer inviable un programa aunque la prueba sea técnicamente excelente.
Eso obliga a salir del laboratorio y del detector. La calidad del programa depende también de si la población acude, confía, entiende para qué sirve la prueba y tolera razonablemente la experiencia. La mamografía no es neutra en ese plano. Hay compresión, ansiedad, miedo al resultado, miedo al falso positivo, incomodidad física, dolor en muchos casos y, en algunos contextos, desconfianza institucional.
Conviene no trivializar esa parte. Las molestias y el dolor no son un detalle secundario sin importancia técnica. Forman parte del equilibrio mismo de la prueba. La compresión mejora inmovilización, reduce superposición tisular, ayuda al contraste, controla espesores y puede contribuir a optimizar dosis y calidad de imagen. Pero esa misma compresión es también una de las razones principales por las que la prueba resulta mal tolerada para muchas pacientes.
La aceptación como límite estructural del cribado
Comparar la mamografía con otras pruebas de cribado ilustra hasta qué punto la aceptación puede ser el factor determinante.
El antígeno prostático específico (PSA) como herramienta de cribado de cáncer de próstata ha tenido una historia más accidentada que la mamografía, en parte por su perfil estadístico — baja especificidad, VPP modesto, riesgo real de sobrediagnóstico — pero también porque el paso de un PSA elevado al procedimiento de confirmación implica una biopsia prostática que muchos hombres rechazan o demoran. El circuito de confirmación forma parte de la aceptabilidad del programa: si la prueba inicial tiene poca carga pero el siguiente paso es muy invasivo o mal tolerado, la participación global cae.
La colonoscopia es otro caso extremo. Su capacidad diagnóstica y preventiva para el cáncer colorrectal es sólida, pero exige preparación intestinal, sedación, tiempo de recuperación y una experiencia que muchas personas encuentran demasiado costosa. Programas que intentaron usarla como prueba de cribado poblacional universal encontraron participaciones muy inferiores a las esperadas. La solución en muchos sistemas fue sustituirla o complementarla con pruebas de menor carga, como la detección de sangre oculta en heces (SOH), que tiene menor coste de participación aunque también menor sensibilidad para lesiones precancerosas.
Esta lógica tiene una consecuencia directa de política sanitaria:
La mamografía ocupa un lugar relativamente favorable en este espectro. No requiere sedación, no es intrínsecamente invasiva, puede realizarse en un tiempo corto y no deja al paciente con restricciones posteriores. Pero eso no la hace neutral: la compresión, el dolor y la ansiedad siguen siendo barreras reales, y en algunos grupos demográficos o culturales la participación es significativamente inferior a la media del programa.
Confianza, accesibilidad y diseño del programa
La aceptación tampoco es igual en todos los sistemas sanitarios ni en todas las culturas de screening. Incluso en poblaciones con perfiles demográficos comparables puede haber diferencias marcadas en participación si cambian la confianza en el sistema, la accesibilidad geográfica, la claridad del circuito o la continuidad entre screening, confirmación y tratamiento.
No conviene simplificar esto a “unos aceptan y otros no”. Lo correcto es decir que la adhesión real depende de confianza, comunicación, accesibilidad y diseño del programa — y que un programa que descuida estas dimensiones fracasa aunque el equipo sea técnicamente excelente.
Por eso el rendimiento real del cribado no depende solo de sensibilidad y especificidad intrínsecas. Depende también de:
- accesibilidad geográfica y logística;
- tiempos de citación y de respuesta al resultado;
- claridad del circuito desde la invitación hasta la confirmación;
- comunicación honesta del beneficio y de los límites de la prueba;
- control razonable de molestias sin degradar innecesariamente la calidad;
- y continuidad entre screening, diagnóstico y tratamiento.
7. Rango de edad, riesgo y a quién se invita
El cribado mamográfico no consiste solo en tener una prueba disponible. Consiste en decidir a quién invitas, cuándo, cada cuánto y con qué excepciones.
Ahí entran dos lógicas que conviven y a veces chocan:
- el cribado poblacional de riesgo medio;
- y los circuitos específicos para personas con mayor riesgo, que a menudo exigen otro seguimiento, otras edades de inicio o incluso otras modalidades complementarias.
En muchos sistemas sanitarios, el rango clásico de cribado poblacional se ha movido históricamente alrededor de la franja de 50 a 69 años cada dos años, pero ese marco se reevalúa de forma periódica. La discusión sobre ampliar edades, incorporar mejor a grupos de alto riesgo o ajustar la intensidad del seguimiento no es una anomalía: es parte normal de cualquier programa serio. Eso es importante porque muestra que la técnica no vive congelada. Se reevalúa según evidencia, capacidad y prioridades.
La pregunta seria no es solo “ampliamos o no ampliamos”. La pregunta seria es:
- si el beneficio adicional justifica el esfuerzo;
- si el sistema puede absorber más volumen sin degradar calidad;
- si hay suficientes radiólogos, técnicos, equipos y circuitos diagnósticos;
- y si la estratificación por riesgo puede hacer el programa más efectivo sin volverlo inmanejable.
Ahí es donde la mamografía se vuelve de verdad un asunto de salud pública y no solo de imagen.
8. Disponibilidad de radiólogos y carga de lectura
La mamografía no termina cuando se adquiere la imagen. Empieza otra fase, y es una fase dura: la lectura.
La interpretación mamográfica exige experiencia, atención sostenida, comparación con estudios previos y una tolerancia muy afinada a la incertidumbre. La dificultad no es solo detectar una masa evidente; la dificultad está muchas veces en decidir cuándo una asimetría merece recall, cuándo una microcalcificación cambia de categoría o cuándo una aparente sospecha no debe arrastrar a una cascada innecesaria.
Eso hace que la mamografía dependa mucho del sistema de lectura:
- número de radiólogos disponibles;
- carga de trabajo;
- doble lectura cuando existe;
- tiempos de respuesta;
- y circuitos de consenso.
Hablar del “problema de los radiólogos” no es una crítica al especialista. Es reconocer que el screening mamográfico escala mucho mejor en la fase de adquisición que en la fase de interpretación. El cuello de botella no siempre es el aparato. Muy a menudo es la lectura experta.
Y ahí la física médica vuelve a aparecer, no como protagonista simbólica, sino como parte de una cadena que tiene que sostener un equilibrio muy delicado entre calidad de imagen, flujo, carga clínica y rendimiento diagnóstico.
11. Validez de la prueba: sensibilidad, especificidad y valor predictivo
La validez de una prueba de cribado no se puede evaluar con una sola métrica. Requiere entender cómo se relacionan cuatro medidas y cómo cambian según el contexto.
En España se diagnosticaron 36.395 casos de cáncer de mama en 2024, según datos de la SEOM y la Red Española de Registros de Cáncer (REDECAN), lo que lo convierte en el cáncer más frecuente en mujeres. La supervivencia a 5 años se sitúa en torno al 86%. El programa nacional de cribado cubre mujeres de 50 a 69 años (con algunas comunidades ampliando ya hacia 45–74), con una participación que ronda el 74–89% de las invitadas, según la fuente y la comunidad autónoma.
Sensibilidad es la capacidad de detectar los casos verdaderos: de cada cien mujeres con cáncer de mama que se someten a la prueba, ¿cuántas obtienen un resultado positivo? En mamografía 2D convencional, la sensibilidad se sitúa típicamente entre el 75 y el 85%; la tomosíntesis (DBT) mejora este valor, especialmente en mamas densas. Una prueba poco sensible deja escapar casos — los falsos negativos.
Especificidad es la capacidad de no alarmar a las sanas: de cada cien mujeres sin cáncer, ¿cuántas obtienen un resultado negativo? En mamografía, la especificidad se sitúa entre el 88 y el 95% según el sistema y el protocolo de lectura. Una prueba poco específica genera recalls y biopsias innecesarios — los falsos positivos.
Hasta aquí parece sencillo. El problema aparece cuando se introduce la prevalencia: la proporción real de enfermedad en la población que se criba.
En cribado mamográfico de población general, la prevalencia de cáncer es baja — del orden de 4–6 casos por 1.000 mujeres invitadas en una ronda de cribado bienal. Una prueba con especificidad del 90% puede sonar excelente. Pero con esa prevalencia, ese 10% de falsos positivos afecta a cerca de 100 mujeres sanas por cada 5 verdaderos positivos. El valor predictivo positivo (VPP) — la probabilidad de que un resultado positivo corresponda a un caso real — es en esas condiciones sorprendentemente bajo, aunque la prueba sea buena.
Esto no es un fallo de la mamografía. Es una consecuencia matemática inevitable de operar con prevalencias bajas. Y tiene implicaciones directas sobre:
- cuántos recalls genera el programa por caso detectado,
- cuántas biopsias resultan benignas,
- y cuánta ansiedad, tiempo y coste consume el proceso de confirmación.
El valor predictivo negativo (VPN) — la probabilidad de que un resultado negativo signifique ausencia real de enfermedad — suele ser alto en cribado, precisamente porque la prevalencia es baja. Pero “suele ser alto” no significa “garantizado”, y una mamografía negativa no cierra el caso si hay síntomas o factores de riesgo relevantes.
En mamografía no basta con decir “hay que detectar más”. Detectar más a cualquier precio puede significar más falsos positivos, más ansiedad, más pruebas adicionales, más biopsias benignas y más presión sobre el sistema.
Por eso el objetivo real no es maximizar una métrica aislada, sino mantener una combinación útil de sensibilidad, especificidad y capacidad operativa para el circuito de confirmación.
10. Derivación diagnóstica y biopsia
Otro motivo por el que la mamografía sigue siendo tan central es que no solo detecta. También orienta el procedimiento posterior.
Cuando aparece un hallazgo sospechoso, la mamografía puede:
- justificar ampliaciones diagnósticas;
- guiar localización de lesiones;
- apoyar procedimientos estereotácticos;
- servir de base para biopsia guiada por imagen;
- y ayudar a planificar el circuito entre cribado, confirmación y decisión terapéutica.
Esto importa mucho en microcalcificaciones y lesiones no palpables. La utilidad clínica de la mamografía no está solo en “ver algo”; está también en permitir que ese algo sea encontrado, caracterizado y, cuando haga falta, muestreado con precisión razonable.
Ahí se ve muy bien que la prueba pertenece al sistema y no solo al aparato. La imagen buena es la que permite la siguiente acción correcta.
11. Calidad regulatoria y MQSA
La mamografía es uno de los mejores ejemplos de cómo una técnica de imagen termina exigiendo un ecosistema regulatorio fuerte. La FDA mantiene documentación específica sobre mamografía y sobre la Mammography Quality Standards Act (MQSA), precisamente porque aquí no basta con que el equipo funcione “más o menos bien”. Hay exigencias sobre dosis, personal, equipamiento, calidad de imagen, acreditación y comunicación a pacientes.
Eso es parte de la historia de éxito de la técnica. La mamografía no se volvió central solo por sus virtudes físicas. Se volvió central también porque el sistema construyó alrededor de ella un marco de calidad reconocible y replicable.
Referencias útiles:
- FDA - Mammography
- FDA - Mammography Quality Standards Act and Program
- FDA - Mammography Information for Patients
- FDA - Important Information on the Final MQSA Rule
- FDA - Digital Breast Tomosynthesis (DBT) System
12. Inteligencia artificial en lectura mamográfica
La IA ha entrado en mamografía por razones obvias. Hay mucho volumen, mucha lectura repetitiva, mucha presión asistencial y mucho valor potencial en detectar antes o en reducir trabajo innecesario.
Pero la promesa interesante no es la más grandilocuente. No se trata de reemplazar al radiólogo con un sistema mágico que decide solo. La promesa seria es más modesta y, por eso mismo, más útil:
- mantener sensibilidad alta;
- mejorar especificidad donde se pueda;
- reducir falsos positivos evitables;
- priorizar casos;
- y ayudar a que el sistema soporte mejor la carga.
Ese último punto es clave. La IA no entra solo por ambición tecnológica. Entra porque en muchos sistemas de salud coinciden varios problemas a la vez:
- más población candidata a cribado,
- posible ampliación de rangos de edad,
- necesidad de atender grupos de mayor riesgo con circuitos diferenciados,
- y capacidad limitada de lectura especializada.
En ese escenario, una IA útil no es la que promete milagros. Es la que ayuda a mantener el rendimiento clínico del programa sin hundirlo por saturación.
Eso encaja muy bien con dos líneas de trabajo que merece la pena citar aquí:
- Evaluation of Combined Artificial Intelligence and Radiologist Assessment to Interpret Screening Mammograms
- Automatic intensity windowing of mammographic images based on a perceptual metric
La primera merece citarse de forma explícita porque resume bien el enfoque: JAMA Network Open publicó Evaluation of Combined Artificial Intelligence and Radiologist Assessment to Interpret Screening Mammograms en la línea de estudiar cómo la combinación entre sistema y radiólogo puede rendir mejor que cada parte por separado, preservando sensibilidad y buscando mejorar especificidad. La segunda recuerda algo más básico, pero igual de importante: antes de la IA ya existía y sigue existiendo mucho trabajo fino en presentación, percepción y calidad de imagen. En mamografía, eso forma parte directa del rendimiento diagnóstico.
Caso guiado: IA en mamografía y retrospectivo local Un ejemplo de despliegue serio donde el retrospectivo local debe ser independiente del entrenamiento del modelo y servir para simular carga, recalls y biopsias sin perder sensibilidad.13. Resumen técnico y organizativo
La mamografía puede describirse como una técnica radiográfica especializada de mama. Eso es correcto, pero se queda muy corto.
Es también:
- una prueba con propiedades estadísticas bien definidas — sensibilidad, especificidad, valor predictivo — que varían con la prevalencia de la población estudiada;
- un sistema de clasificación probabilística de hallazgos — no un diagnóstico — que debe ser interpretado en contexto clínico;
- una condición necesaria pero no suficiente para el diagnóstico, que siempre requiere confirmación histológica;
- un programa de salud pública que debe cumplir los criterios de Wilson y Jungner para justificarse éticamente;
- una tecnología regulada bajo marcos específicos como la MQSA;
- y un problema continuo de equilibrio entre beneficio, daño y recursos.
Por eso, dentro de la física médica, la mamografía obliga a mirar más allá del detector. Obliga a pensar en qué mide la prueba, qué no mide, qué infiere, qué garantiza y qué deja abierto para el proceso de confirmación.
Su valor no depende solo de producir una imagen útil. Depende de que esa imagen se interprete correctamente — como signo, no como diagnóstico — y de que el sistema que la rodea pueda completar el proceso de forma eficaz y segura.
Relacionado
- La radiación en medicina
- La radiografía
- La estadística en medicina
- Visualización y procesamiento de imagen
Para ampliar
- FDA - Mammography
- FDA - Mammography Quality Standards Act and Program
- NCI - Breast Cancer Screening (PDQ)
- SEER - Breast Cancer Stat Facts
- WHO - Screening for Breast Cancer
- Wilson & Jungner - Principles and Practice of Screening for Disease (OMS, 1968): el documento fundacional de los criterios de cribado, todavía la referencia más citada en salud pública para evaluar si un programa de screening está justificado.
- NCI - Mammograms
- JAMA Network Open - Evaluation of Combined Artificial Intelligence and Radiologist Assessment to Interpret Screening Mammograms
- Medical Physics - Automatic intensity windowing of mammographic images based on a perceptual metric
- NCI Dictionary - Digital Breast Tomosynthesis
- MedPhysics.i-do.science - Publications