La radiación en medicina
La palabra radiación parece simple hasta que uno empieza a usarla en serio. En física médica no nombra una sola cosa. Nombra una familia de fenómenos, fuentes, haces y estrategias técnicas que comparten una idea general, sí, pero no la misma física fina ni el mismo uso clínico.
No es lo mismo un tubo de rayos X que una fuente radiactiva sellada. No es lo mismo un fotón de aniquilación en PET que un haz de megavoltaje en radioterapia. No es lo mismo un campo de protones que una radiografía de tórax.
Y precisamente por eso conviene poner aquí una pieza base.
Porque antes de discutir radiografía, mamografía, TAC, PET, braquiterapia o protonterapia, merece la pena dejar clara una idea sencilla: en medicina no usamos “radiación” en abstracto. Usamos radiaciones concretas, producidas de formas distintas, con espectros distintos, interacciones distintas y consecuencias clínicas distintas.
1. Tipos de radiación usados en medicina
Una primera separación útil es esta:
- fotones, como rayos X y gamma;
- partículas cargadas, como electrones o protones;
- y, en algunos contextos más específicos, otras partículas o emisiones secundarias que acompañan a los procesos principales.
Los fotones no tienen masa en reposo ni carga eléctrica. Interactúan estadísticamente con la materia y pueden atravesarla con mayor o menor probabilidad según energía, espesor y composición.
Las partículas cargadas, en cambio, sí tienen masa y carga. Pierden energía de otro modo, siguen trayectorias más condicionadas por el medio y pueden concentrar depósito energético con una lógica muy distinta.
Esa diferencia ya ordena medio campo.
2. Fotones en imagen y terapia
En términos físicos, rayos X y rayos gamma son ambas cosas fotones. La diferencia clásica no está en “qué son”, sino en de dónde salen.
- Los rayos X suelen asociarse a procesos electrónicos y a producción artificial en tubos o aceleradores.
- Los gamma suelen asociarse a transiciones nucleares de radionúclidos o fuentes radiactivas.
No conviene exagerar esta frontera como si separara dos mundos incomunicables. La física de interacción con la materia tiene mucho terreno común. Pero la diferencia de origen importa muchísimo en clínica, porque cambia:
- la forma de producir la radiación;
- el espectro disponible;
- la geometría del haz;
- la logística del sistema;
- la dosimetría;
- y el tipo de control técnico necesario.
3. De dónde salen los rayos X: bremsstrahlung y radiación característica
Cuando en radiología hablamos de un tubo de rayos X, la idea física central es bastante elegante.
Primero aceleramos electrones mediante una diferencia de potencial alta. Luego esos electrones impactan contra un blanco metálico, normalmente de alto número atómico. En ese choque aparecen dos componentes importantes.
La primera es la radiación de frenado o bremsstrahlung. El electrón llega rápido, se desacelera en el campo coulombiano de los núcleos del blanco y emite fotones con una distribución continua de energías. Ese continuo es una de las claves del problema.
La segunda es la radiación característica. Si el impacto reorganiza la estructura electrónica del material del ánodo, aparecen fotones con energías discretas propias de ese elemento.
Por eso el haz de rayos X clínico no suele ser monoenergético. Es, en general, un haz policromático.
Y esto no vale solo para diagnóstico. En radioterapia externa con aceleradores lineales, cuando usamos electrones de alta energía contra un blanco para producir fotones de megavoltaje, volvemos a usar, en esencia, bremsstrahlung. Cambia la escala energética. La idea física de fondo sigue siendo reconocible.
4. Interacción de fotones con la materia
Que un fotón atraviese el cuerpo no significa que lo haga siempre de la misma manera. La interacción dominante cambia con la energía y con el material.
En diagnóstico, dos nombres bastan para ordenar mucho:
- efecto fotoeléctrico
- dispersión Compton
El fotoeléctrico favorece más el contraste diferencial y pesa mucho cuando las energías son relativamente bajas y el material tiene número atómico efectivo mayor. Por eso resulta tan importante en radiografía, mamografía y en todo lo que depende de sacar partido a diferencias finas de atenuación.
Compton, en cambio, gana terreno cuando sube la energía y cuando el problema se parece más a “atravesar masa” que a distinguir composición fina. Ahí la señal puede seguir llegando, sí, pero el contraste útil entre tejidos se vuelve más ingrato y además aparece más dispersión.
Dicho de forma simple: no todo fotón que cruza el cuerpo ayuda igual a formar una imagen útil.
5. Espectro, filtración y endurecimiento del haz
Como el haz de rayos X es policromático, los fotones de baja energía no se comportan igual que los de energía más alta.
Los más blandos se absorben con facilidad y muchas veces aportan más a la dosis superficial que a la señal útil en el detector. Por eso se filtran. Esa filtración no es un detalle menor. Es parte del diseño físico del haz.
Y luego aparece otro fenómeno clave: el endurecimiento del haz.
Cuando el haz atraviesa materia, los fotones de menor energía son retirados preferentemente. El resultado es que la energía media del haz que sigue adelante aumenta. El haz “se endurece”.
Eso tiene varias consecuencias:
- cambia el contraste efectivo a lo largo del espesor;
- hace que la misma anatomía no se vea igual en trayectos cortos y largos;
- complica la linealidad intuitiva entre espesor y gris;
- y en tomografía puede introducir artefactos o sesgos si no se corrige bien.
Es una de esas ideas que parecen accesorias hasta que uno intenta cuantificar de verdad.
6. Penetración, contraste, señal y dosis
Aquí aparece una de esas situaciones en las que no se puede maximizar todo a la vez.
Las energías más bajas suelen dar más contraste radiográfico porque la atenuación diferencial entre tejidos aumenta. Si trabajamos con kilovoltajes más bajos, los tejidos blandos pueden separarse mejor, especialmente cuando la anatomía lo permite y la geometría está bien elegida.
Pero esa ventaja tiene precio.
Con energías más bajas:
- el haz penetra peor;
- llega menos señal al detector;
- y si queremos sostener la calidad de imagen quizá tengamos que aumentar carga o tiempo.
Y ahí aparece la frase incómoda, pero física: si uno se obsesiona con bajar energía para exprimir contraste, puede terminar pagándolo en dosis.
En el otro extremo, con energías más altas:
- ganamos penetración;
- atravesamos espesores mayores con más facilidad;
- pero el contraste diferencial se aplana.
En presencia de hueso, además, el problema se vuelve todavía más duro. A cierta energía uno atraviesa mejor, sí, pero también puede perder la separación fina entre tejidos blandos próximos a estructuras muy atenuantes. Por eso no existe un “mejor kV” universal. Cada tarea clínica obliga a ordenar prioridades distintas.
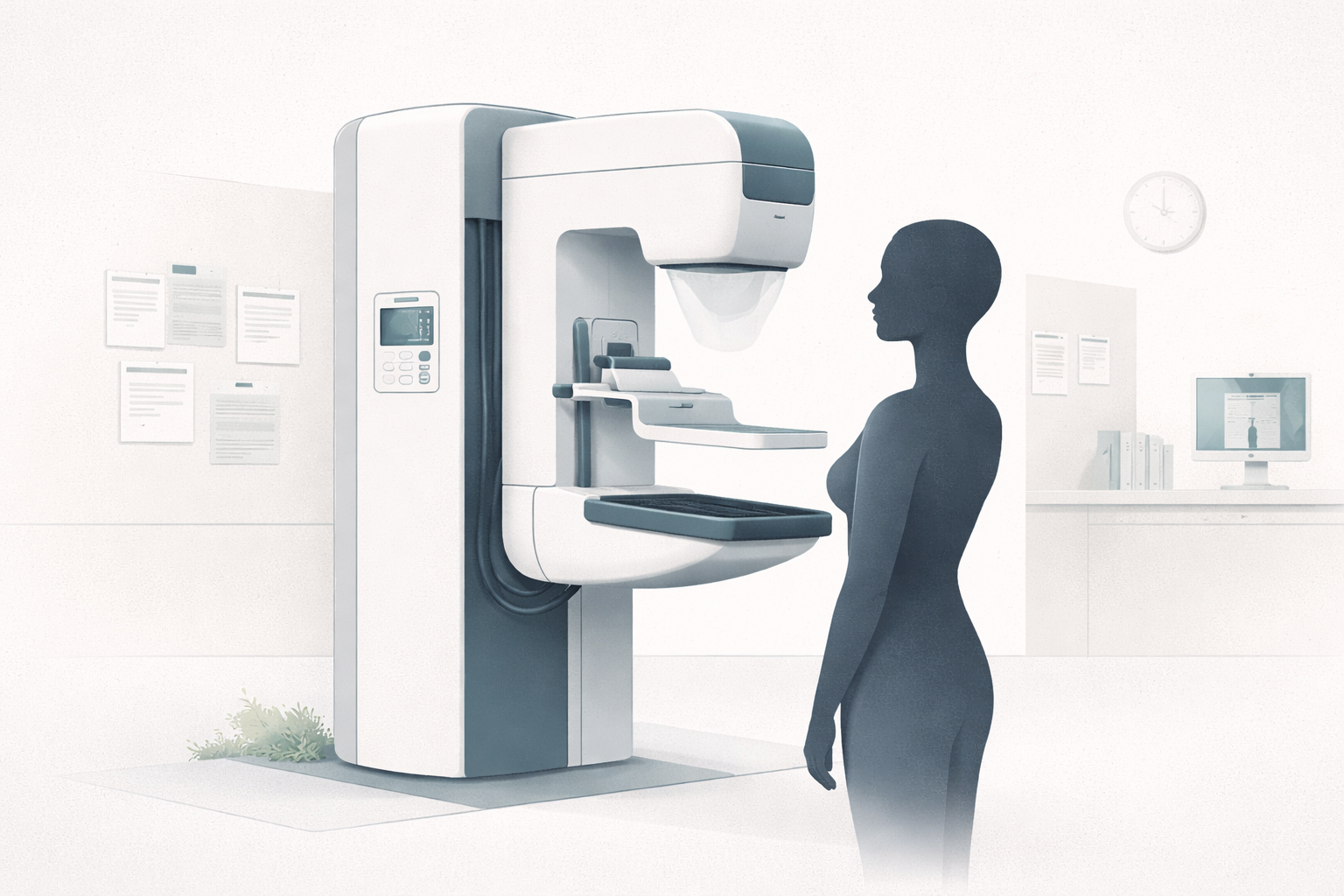
La mamografía entiende esto de forma especialmente fina. También la radiografía general, el tórax, la fluoroscopia y el TAC, cada una a su manera.
7. Dual-energy y densitometría: aprovechar la dependencia energética
Una de las consecuencias más bonitas de esta física es que la atenuación depende de la energía. Y si depende de la energía, entonces podemos intentar explotar esa diferencia.
Ahí entran las técnicas dual-energy y, de forma muy clásica y madura, la densitometría ósea por DXA / DEXA.
La idea de fondo es esta:
- usar dos espectros o dos niveles energéticos distintos;
- medir cómo cambia la atenuación;
- y separar mejor contribuciones de materiales o tejidos que no responden igual a ambas energías.
En densitometría ósea eso permite estimar con mucha más inteligencia la contribución mineral ósea frente al tejido blando superpuesto. No es una simple radiografía repetida. Es un uso deliberado de la dependencia energética de la atenuación.
La misma familia conceptual reaparece después en otras técnicas, incluida parte del mundo de la tomografía dual-energy y de la descomposición material.
8. Radionúclidos, braquiterapia y PET
Aquí cambiamos de lógica. Ya no estamos generando un haz en un tubo. Estamos trabajando con radionúclidos.
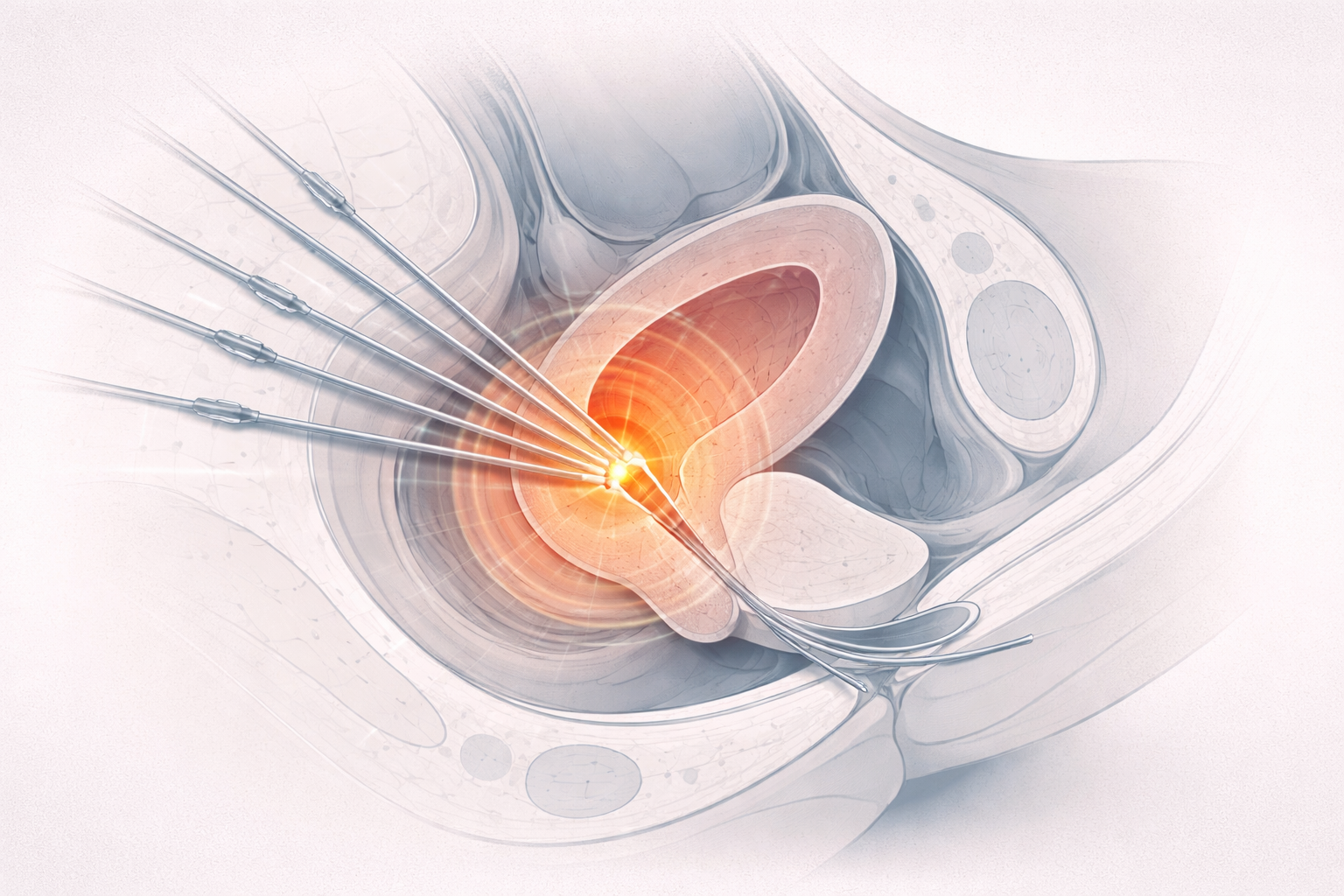
En braquiterapia, por ejemplo, el problema físico incluye:
- actividad de la fuente;
- decaimiento temporal;
- emisiones asociadas al radionúclido;
- geometría de colocación;
- y seguridad de manejo.
Históricamente, en radioterapia también han existido equipos gamma basados en fuentes como cobalto-60, y en radiocirugía eso ha dejado una huella técnica muy clara.
En medicina nuclear diagnóstica aparece otra variante. El PET no usa un tubo de rayos X externo. Usa radionúclidos que participan en decaimientos donde interviene emisión de positrones. Y lo que el sistema detecta finalmente son los dos fotones de aniquilación de 511 keV generados cuando ese positrón se encuentra con un electrón.
Eso cambia por completo la pregunta técnica:
- ya no es “qué haz le mando al paciente”;
- sino “qué actividad administro, cómo se distribuye y qué fotones salen desde dentro”.
Por eso PET, braquiterapia y radioterapia con fuentes comparten una intuición importante: la radiación aquí no se entiende sin decaimiento radiactivo, actividad, vida media y logística isotópica.
9. Aceleradores y generación de haces
Otra gran familia de la física médica es la de los aceleradores.
Un acelerador lineal clínico puede hacer dos cosas principales:
- acelerar electrones y usarlos como haz terapéutico;
- o hacer que esos electrones impacten en un blanco para generar fotones de alta energía por bremsstrahlung.
Es decir: parte de la radioterapia moderna vuelve a pasar por la misma idea física que ya estaba en el tubo de rayos X, aunque a otra escala energética y con otra arquitectura técnica.
Los protones abren otro camino. Para ellos necesitamos aceleradores de partículas como ciclotrones o sincrotrones, además de toda la línea de transporte, selección energética, escaneo y entrega.
Y esta familia no importa solo para tratamiento. También aparece en la producción de radionúclidos, por ejemplo cuando un ciclotrón abastece parte del ecosistema necesario para PET.
En otras palabras: la física de aceleradores no es una rareza lateral del hospital moderno. Es una de sus infraestructuras profundas.
10. Protones: otra física de depósito de dosis
Los protones no son fotones. Y esa diferencia se nota muchísimo.
Tienen masa, tienen carga y pierden energía a lo largo del recorrido con una lógica que permite un rango finito y un máximo de depósito energético cercano al final de trayectoria, el famoso pico de Bragg.
Eso los vuelve muy atractivos cuando interesa concentrar dosis y limitar salida distal. Pero esa elegancia tiene condiciones:
- sensibilidad a heterogeneidades;
- dependencia fuerte de la densidad efectiva recorrida;
- necesidad de control geométrico e imagen especialmente rigurosos;
- y complejidad tecnológica y económica muy superior.
Por eso protones no significa “radiación mejor” en abstracto. Significa otra física, con ventajas concretas y exigencias concretas.
11. Resumen técnico
Esta pieza no pretende cerrar el tema. Pretende ordenar el resto.
Porque después de esto ya se entiende mejor por qué:
- la radiografía y la mamografía viven tan pendientes del espectro y del contraste;
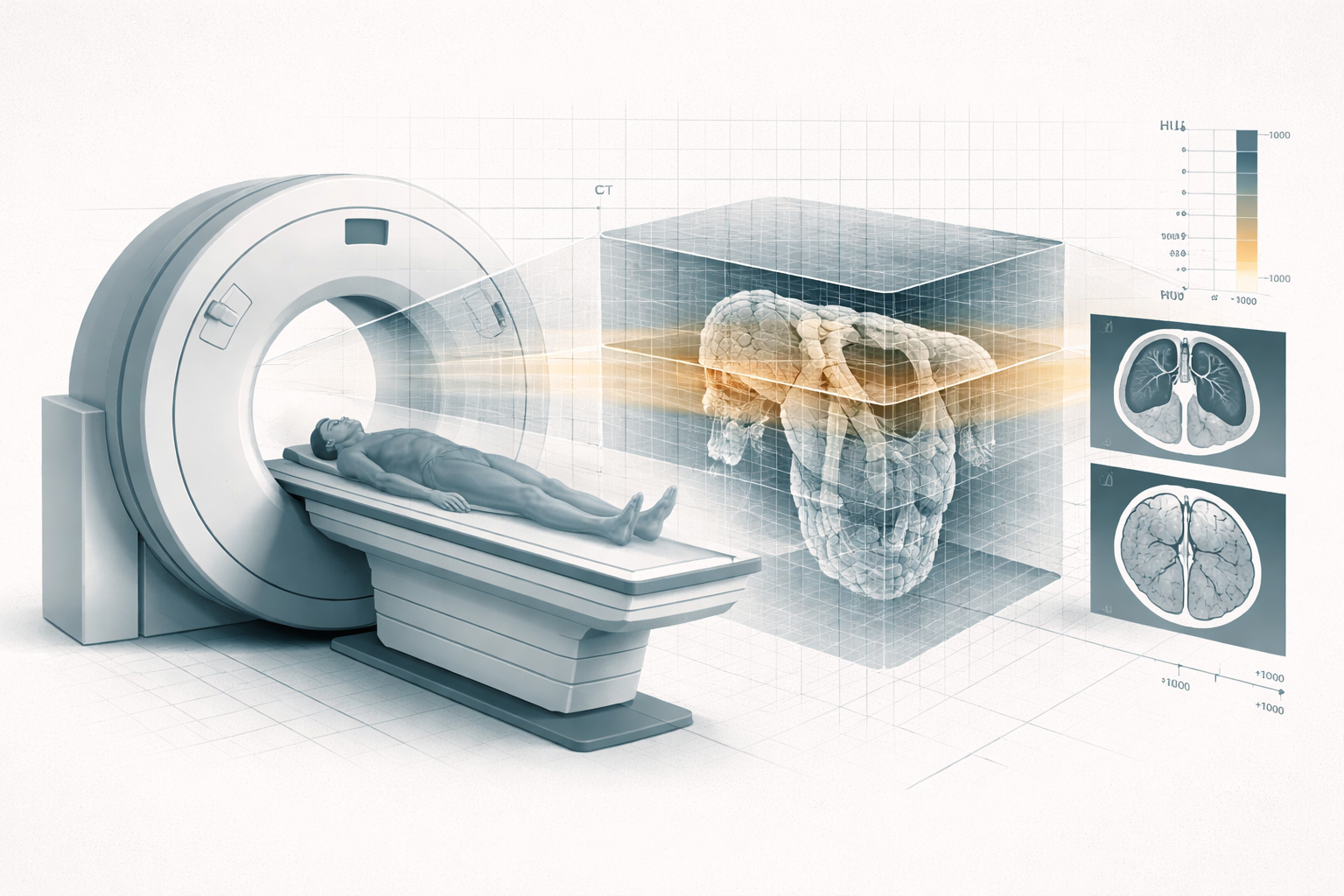
- el TAC necesita corregir endurecimiento del haz y cuantificar bien;
- la densitometría usa dos energías;
- PET depende de radionúclidos, actividad y fotones de aniquilación;
- la braquiterapia vive del decaimiento de fuentes;
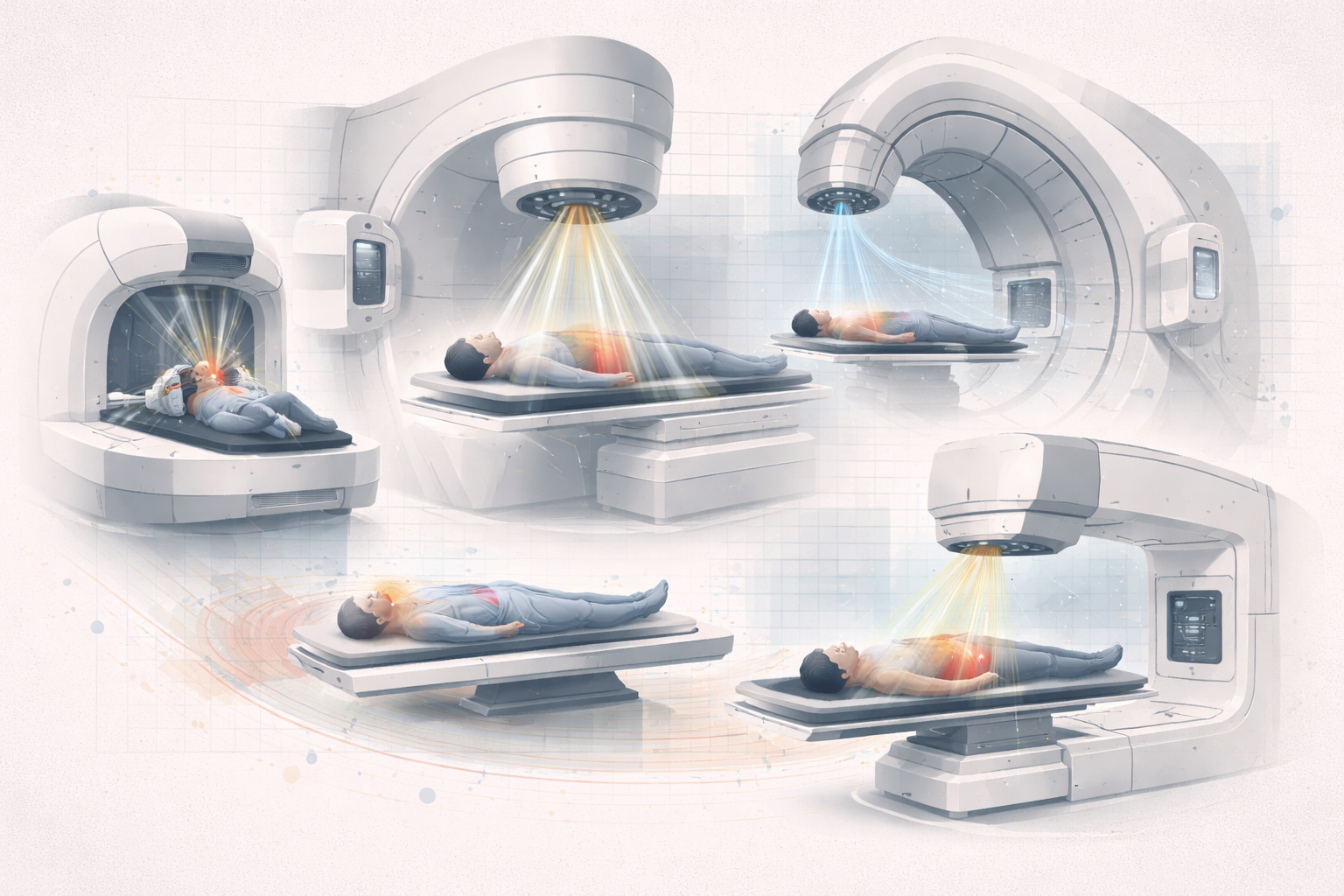
- y la radioterapia externa puede trabajar con electrones, fotones o protones según otra lógica completamente distinta.
Al final, la palabra radiación sirve, sí. Pero se queda muy corta si no añadimos inmediatamente otra pregunta:
qué radiación, producida cómo, con qué espectro y para qué problema clínico.
Y quizá esa sea la mejor razón para colocar este texto al principio del bloque.