La imagen tisular
La imagen tisular cubre una familia de técnicas donde la información clínica procede de tejido visible, secciones histológicas, preparación de muestras, microscopia y digitalización de muy alta resolución.
En este grupo ya no estamos, en general, ante grandes escáneres corporales ni ante una anatomía vista desde fuera. Estamos ante tejidos, cortes, contraste visible, preparación de muestras, microscopia y cantidades muy grandes de información visual. Cambia la escala, cambia el tipo de contraste y cambia también la infraestructura necesaria para adquirir, archivar y procesar la imagen.
1. Una imagen visible, pero nada simple
La imagen tisular suele parecer intuitiva porque es, muchas veces, imagen visible. Se ven color, textura, forma, contraste y estructuras reconocibles. En piel, mucosa, secciones histológicas o muestras teñidas, la lectura visual entra antes que en TAC o PET.
Precisamente por eso conviene separar apariencia visual y cadena técnica.
Que una imagen sea visible no significa que sea inmediata. Entre el tejido y la imagen final puede haber:
- obtención de muestra;
- fijación;
- inclusión;
- corte;
- tinción;
- escaneado;
- corrección de color;
- ensamblado digital;
- y, cada vez más, procesado automatizado.
La imagen tisular no es solo observación microscópica. Es una cadena técnica compleja para producir una imagen interpretable.
2. De la superficie al corte fino
Aquí caben varias escalas y conviene distinguirlas.
Por un lado están las imágenes más directamente visibles de tejido o superficie, como ciertas exploraciones de piel, mucosa o superficies quirúrgicas. Ahí la pregunta puede ser morfológica a ojo, fotográfica o apoyada por aumentos modestos.
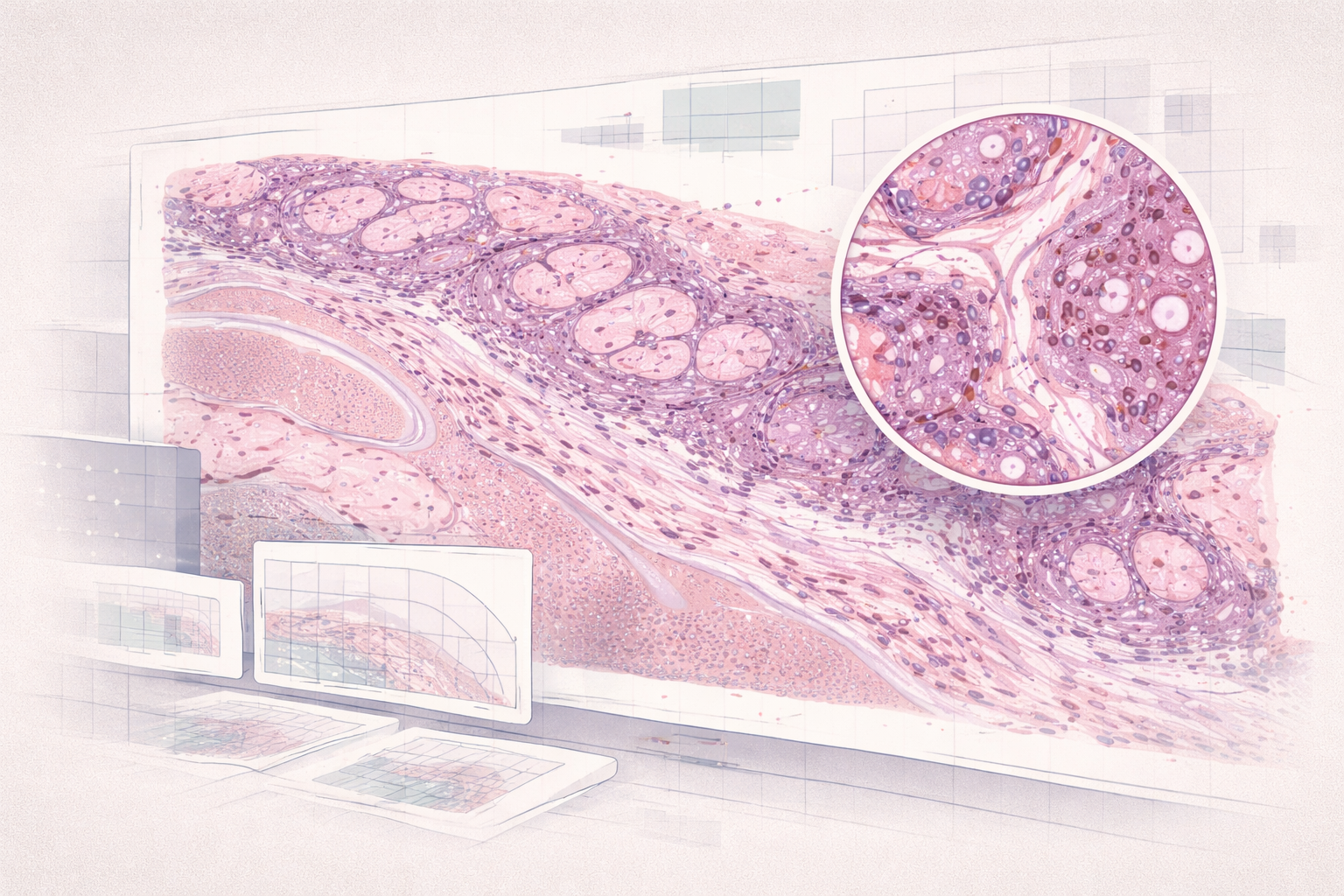
Por otro lado está la gran tradición de la histología y de la patología digital, donde el tejido se corta en secciones muy finas y se observa con enorme resolución. Ahí ya no estamos viendo solo una lesión macroscópica. Estamos viendo organización tisular, células, núcleos, arquitectura, infiltración, bordes y patrones que el ojo entrenado del patólogo lleva décadas aprendiendo a distinguir.
Ese paso es muy importante. La medicina deja de preguntar solo “qué masa hay” o “dónde está el tumor” y empieza a preguntar también “qué tipo de tejido es esto”, “cómo está organizado” y “qué características microscópicas sostienen un diagnóstico o una clasificación”.
3. El contraste aquí no viene de la atenuación: viene de la preparación
En radiografía o TAC hablábamos de atenuación. En RM, de señal. En ultrasonidos, de ecos. En imagen tisular el contraste suele venir, sobre todo, de otra parte: de la preparación de la muestra.
El tejido hay que hacerlo legible.
Eso significa usar medios físicos, químicos y ópticos que resalten estructuras que a simple vista no se separarían con suficiente claridad. Tinciones como hematoxilina-eosina, técnicas inmunohistoquímicas, fluorescencia u otras estrategias específicas hacen visible lo que de otra forma quedaría demasiado mezclado o demasiado uniforme.
Aquí el contraste no está solo en el objeto ni solo en el detector. Depende también de una intervención previa sobre la muestra que modifica su legibilidad.
Por eso la imagen tisular requiere medios de procesado muy especiales. No basta con adquirir. Hay que preparar, revelar, seleccionar el contraste correcto y, a menudo, volver a escanear o reinterpretar según la pregunta diagnóstica.
4. Resolución enorme, archivos enormes
Una de las grandes diferencias con otras modalidades es la escala de la resolución.
La imagen tisular digital moderna, y en particular la whole-slide imaging, genera archivos gigantescos. No es raro que una sola preparación escaneada a gran aumento produzca una imagen con un número de píxeles enorme, muy por encima de lo que la intuición cotidiana asocia a “una foto médica”.
Eso tiene consecuencias muy prácticas:
- almacenamiento serio;
- transmisión de datos no trivial;
- necesidad de formatos adecuados;
- visualización por niveles de zoom;
- y una relación nueva entre imagen y computación.
Aquí la física se cruza enseguida con la informática. La imagen tisular no solo exige buen contraste y buena óptica. Exige infraestructura de datos.
5. Arquitectura tisular y organización espacial
En este campo el interés no está solo en la célula aislada. Está también en la arquitectura tisular.
En muchos diagnósticos importa:
- la distribución de núcleos;
- la relación entre estroma y célula tumoral;
- la presencia de necrosis;
- el borde infiltrativo;
- la forma de la glándula o del epitelio;
- la densidad celular;
- la vascularización visible;
- y una larga lista de patrones que mezclan escala celular y escala de tejido.
Eso convierte a la imagen tisular en un terreno especialmente útil para clasificación y cuantificación. No solo por resolución, sino por organización espacial.
6. Inteligencia artificial: automatización y requisitos de datos
Si en radiología la IA promete ayudar mucho, en imagen tisular la tentación de automatizar es todavía mayor. Y tiene bastante lógica.
Aquí hay:
- imágenes enormes;
- flujo continuo de muestras;
- tareas repetitivas;
- patrones visuales complejos;
- y una necesidad constante de segmentar, clasificar, contar, detectar o priorizar.
Eso convierte a la patología digital y a la imagen tisular en un terreno muy natural para la inteligencia artificial.
Pero también en uno muy exigente.
Porque detrás de cada modelo útil hay una parte muy grande de trabajo de entrada:
- adquisición continua de muestras;
- estandarización de escaneo;
- control del color y de la tinción;
- anotación experta;
- segmentación manual o semiautomática;
- validación;
- y adaptación a datos nuevos que nunca llegan completamente limpios ni homogéneos.
Aquí la IA no aparece como un sistema autónomo que interpreta tejido sin contexto. Aparece como una capa de automatización que necesita disciplina previa para no amplificar errores, sesgos de muestreo o variaciones de laboratorio.
7. Flujo continuo de muestras
Hay además una característica organizativa que hace este campo especialmente interesante. La entrada de muestras es continua.
En radiología uno piensa en listas de pacientes y pruebas. En imagen tisular, especialmente en entornos hospitalarios grandes, aparece además un flujo continuo de biopsias, piezas quirúrgicas, bloques, cortes y preparaciones. Eso convierte la digitalización, el archivo, la lectura y el análisis en infraestructura clínica estable.
Y cuando esa infraestructura se digitaliza, la pregunta ya no es solo diagnóstica. También es computacional:
- cómo almacenar;
- cómo indexar;
- cómo compartir;
- cómo anotar;
- cómo recuperar regiones de interés;
- cómo garantizar consistencia entre centros;
- y cómo entrenar sistemas que no se rompan en cuanto cambia el escáner, la tinción o el protocolo.
8. Relación con otras modalidades de imagen
La imagen tisular no pertenece a la radiología en sentido estricto, pero sí forma parte de la imagen médica.
Existe una medicina de la imagen basada en luz visible, cortes, tinciones, óptica y resolución muy alta. En ella el diagnóstico depende de la morfología fina, de la organización del tejido y de la capacidad de convertir una muestra física en imagen computable.
Eso justifica una pieza específica dentro del bloque.
9. Resumen técnico
La imagen tisular fija varias ideas importantes:
- qué entendemos por imagen médica;
- qué papel juega el contraste cuando no depende solo del equipo;
- cómo cambia la escala cuando dejamos el órgano y entramos en el tejido;
- y cómo la inteligencia artificial, aquí más que en muchos otros lugares, depende de un trabajo previo enorme de adquisición, anotación y control.
Por eso esta modalidad encaja en el bloque aunque no use la misma física de adquisición que TAC o PET. Sigue siendo imagen médica, pero en otra escala y con otra cadena técnica.
Relacionado
- Visualización y procesamiento de imagen
- El PET
- IT, interoperabilidad y datos
- Personal y flujos de trabajo
- La estadística en medicina