Radioterapia
La radioterapia integra física, imagen, geometría, cálculo y responsabilidad clínica en un mismo sistema operativo.
En radioterapia, la física no se limita a describir o reconstruir, sino que se aplica directamente al tratamiento. Se utiliza para depositar una dosis suficientemente alta en un volumen tumoral y, simultáneamente, mantener bajo control la dosis en tejidos sanos. Ese equilibrio surge de una cadena completa de imagen, posicionamiento, delineación, planificación, verificación, medidas, control de calidad y revisión continua.
En este contexto, el papel del físico médico es estructural dentro del sistema clínico y técnico.
1. De la imagen al tratamiento
La radioterapia no empieza cuando el acelerador se enciende. Empieza bastante antes.
Empieza con el diagnóstico, con la extensión de la enfermedad, con la decisión de si el paciente puede beneficiarse de un tratamiento local y con la pregunta más importante de todas: qué queremos controlar, curar o aliviar.
A partir de ahí se encadena un proceso muy propio:
- adquisición de imagen para simulación;
- inmovilización y posicionamiento reproducible;
- definición de volúmenes objetivo y órganos de riesgo;
- planificación dosimétrica;
- prescripción;
- verificación previa;
- tratamiento fraccionado o estereotáctico;
- controles durante el curso del tratamiento;
- y evaluación posterior.
La radioterapia no puede reducirse a la entrega de radiación. Lo que hace es convertir información anatómica, funcional y geométrica en una intervención de alta precisión.
2. Indicaciones clínicas
La radioterapia funciona especialmente bien cuando el problema clínico conserva un componente local o locorregional suficientemente claro.
Eso explica su papel en muchos tumores de:
- cerebro;
- cabeza y cuello;
- mama;
- pulmón;
- próstata;
- recto;
- cérvix;
- piel;
- algunos sarcomas;
- metástasis limitadas;
- y bastantes escenarios paliativos donde el objetivo no es curar, sino reducir dolor, sangrado, compresión o carga sintomática.
No todas las enfermedades se benefician igual. No todos los tumores se comportan igual. No todas las localizaciones toleran la misma agresividad dosimétrica. Pero allí donde existe una diana espacial razonablemente definible, la radioterapia puede ser extremadamente eficaz.
3. Toxicidad, localización y límites clínicos
La radioterapia tiene una lógica profundamente local. Eso explica tanto su potencia como sus límites.
Cuando la enfermedad está localizada o conserva un componente locorregional dominante, la radioterapia puede encajar muy bien. Cuando el problema principal es una enfermedad ampliamente metastásica, su papel suele cambiar: deja de ser una herramienta de control global y pasa más a menudo a escenarios paliativos o de control sintomático muy concreto.
Aquí aparece una diferencia importante frente a tratamientos sistémicos como la quimioterapia. La quimioterapia circula y actúa de forma más general, con toxicidades también generales. La radioterapia, en cambio, concentra su efecto en una región anatómica. Por eso sus efectos adversos suelen estar mucho más ligados al territorio tratado.
Esto no implica ausencia de riesgo, sino una distribución espacial específica de la toxicidad.
Entre los efectos secundarios más conocidos están:
- eritema o enrojecimiento cutáneo;
- mucositis o inflamación de mucosas;
- fatiga;
- caída de pelo cuando el campo incluye zonas pilosas;
- alteraciones digestivas o urinarias según el volumen tratado;
- y toxicidades tardías asociadas a fibrosis, lesión funcional o daño acumulado en órganos concretos.
La radioterapia no se elige solo porque pueda matar células tumorales. Se elige cuando el equilibrio entre beneficio local, toxicidad esperable y alternativas sistémicas o quirúrgicas tiene sentido para ese paciente.
4. Pediatría, supervivencia y segundos cánceres
En población pediátrica esta discusión se vuelve todavía más delicada.
El cuerpo está en desarrollo, la expectativa de vida tras el tratamiento puede ser muy larga y, precisamente por eso, pesan mucho más los efectos tardíos: crecimiento, neurodesarrollo, función endocrina, fertilidad, toxicidades acumuladas y riesgo de segundos tumores radioinducidos.
Ese problema no pertenece solo a la radioterapia. También muchos tratamientos sistémicos, incluida parte de la quimioterapia, pueden aumentar el riesgo de neoplasias secundarias o dejar secuelas tardías importantes. Pero en radioterapia la relación entre volumen irradiado, edad, tejido sano expuesto y horizonte temporal hace que la planificación pediátrica exija un nivel especialmente fino de prudencia.
Ahí se entiende muy bien una idea que atraviesa toda la oncología moderna: no basta con mejorar resultados inmediatos. Hay que pensar también en supervivencia a cinco años, supervivencia prolongada y calidad de esa supervivencia. Tratar mejor no es solo controlar el tumor hoy. Es también reducir el precio biológico que el tratamiento deja para mañana.
5. Familias técnicas de tratamiento
Las dos grandes familias siguen siendo muy claras.
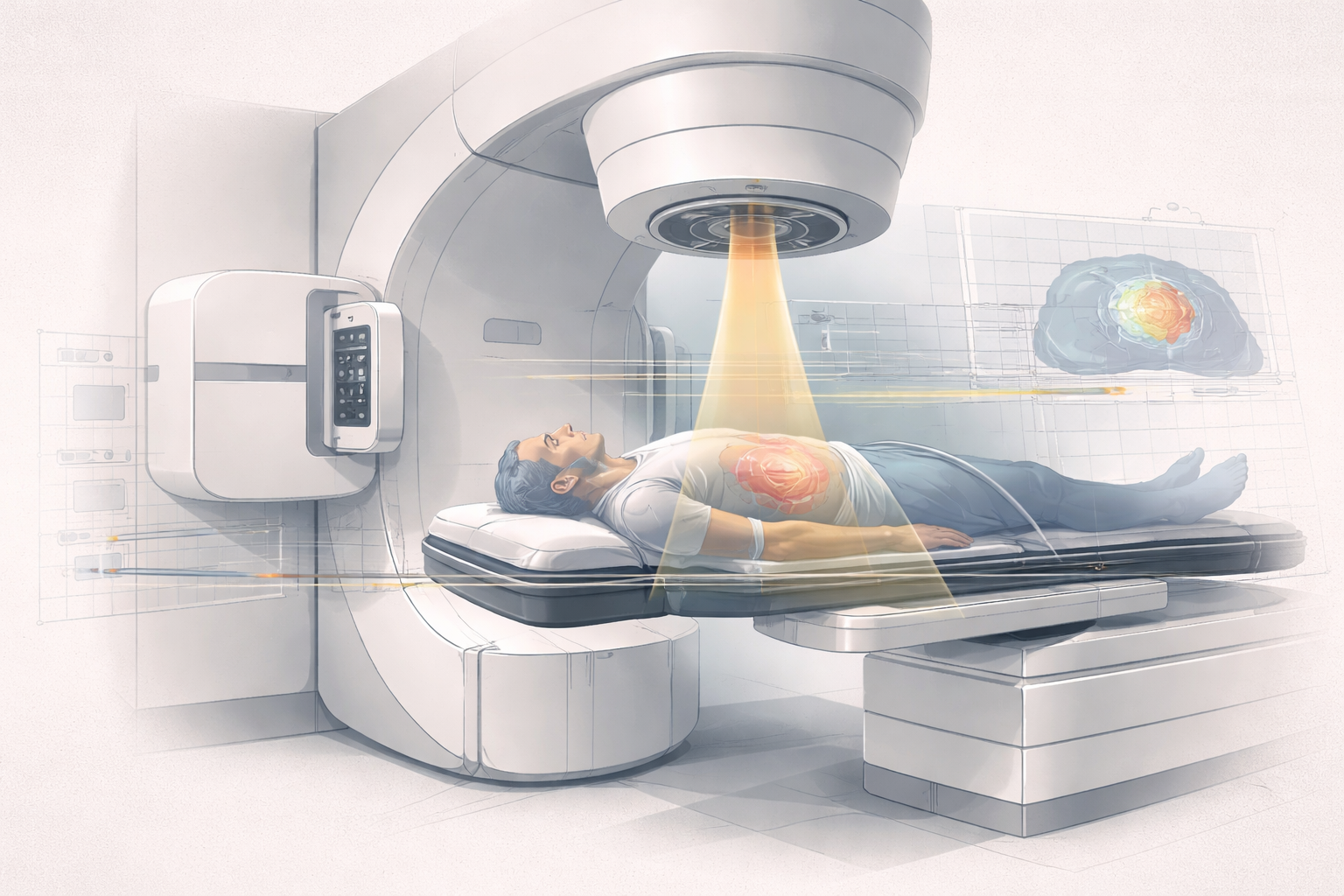
Radioterapia externa
La fuente está fuera del paciente. El haz se genera en un equipo externo y atraviesa el cuerpo hasta alcanzar el volumen objetivo. Aquí entran la teleterapia clásica, los aceleradores lineales modernos, la radiocirugía y muchas variantes de tratamiento conformado o modulado.
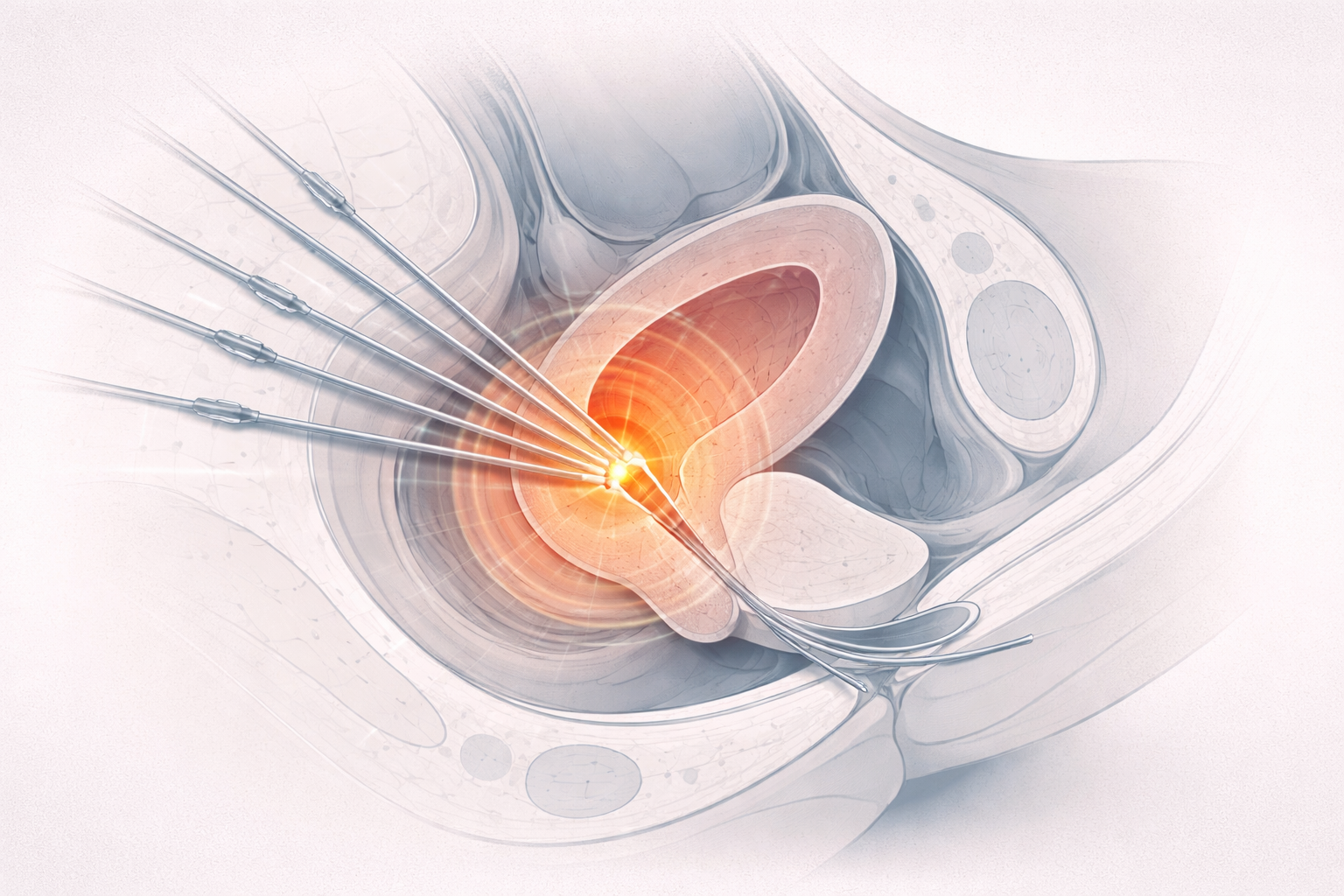
Braquiterapia
La fuente está dentro del paciente o muy cerca del volumen a tratar. Esto cambia radicalmente la geometría y la caída de dosis. Es una técnica especialmente potente cuando interesa una dosis muy alta localizada con rápido descenso alrededor.
Otras variantes
A partir de ahí aparecen muchas familias técnicas:
- radioterapia conformada 3D;
- IMRT (
intensity-modulated radiotherapy, radioterapia de intensidad modulada) y VMAT (volumetric modulated arc therapy, terapia de arco volumétrico modulado); - radioterapia guiada por imagen o IGRT (
image-guided radiotherapy); - radiocirugía y SBRT (
stereotactic body radiotherapy, radioterapia estereotáctica corporal); - radioterapia intraoperatoria;
- protonterapia y otras terapias con partículas;
- y técnicas históricas o aún activas basadas en fuentes radiactivas como cobaltoterapia o sistemas dedicados tipo Gamma Knife.
No hace falta contarlas todas aquí una por una para entender lo esencial: todas intentan mejorar la misma ecuación entre dosis al objetivo y protección del tejido sano.
Caso guiado: próstata y la dificultad de comparar braqui, fotones y protones Incluso en un tumor frecuente, comparar familias de tratamiento exige separar riesgo, hormonoterapia, técnica, toxicidad y años de seguimiento. Caso guiado: la trastienda del equipo de física médica Fuentes, haces, cubas de agua, OAR, isocentro y láseres: el trabajo invisible que hace entregable un plan antes de tratar al paciente. Caso guiado: una planificación completa de radioterapia Desde el TAC de simulación y el contorneo hasta el IGRT diario, la adaptación y el seguimiento clínico de una serie real de tratamiento.6. Volúmenes objetivo y órganos de riesgo
Una parte muy importante del lenguaje de la radioterapia se escribe con siglas. Merece la pena entenderlas porque son la forma más compacta de describir qué queremos tratar y con qué margen.
- GTV (
Gross Tumor Volume): el volumen tumoral visible o demostrable. - CTV (
Clinical Target Volume): el GTV más las zonas donde existe riesgo clínico de enfermedad microscópica. - ITV (
Internal Target Volume): incorpora variaciones internas, por ejemplo movimiento respiratorio. - PTV (
Planning Target Volume): añade márgenes para incertidumbres de posicionamiento, movimiento y entrega. - OAR (
Organs At Risk): órganos o estructuras cuya tolerancia condiciona el tratamiento.
Aquí se ve muy bien por qué la radioterapia es geometría clínica y no solo tecnología. El tratamiento no se dirige al “tumor” como abstracción. Se dirige a un volumen definido con imagen, contexto biológico e incertidumbre espacial.
7. Geometría del paciente e inmovilización
En radioterapia externa no tratamos solo un tumor. Tratamos un tumor en una posición concreta, dentro de un paciente concreto, sobre una mesa concreta, con un aparato que tiene límites geométricos concretos.
Esto requiere considerar:
- inmovilización;
- reproducibilidad del centrado;
- ángulos del gantry;
- recorrido de la mesa;
- colisiones posibles;
- accesibilidad del haz;
- superficie del paciente;
- prótesis o dispositivos;
- y movimiento interno.
La superficie del paciente tiene además un papel cada vez más visible en técnicas de posicionamiento y verificación, especialmente con sistemas de surface imaging en tratamientos externos. En algunos escenarios, la superficie no solo ayuda a colocar. Ayuda a vigilar durante el tratamiento si el paciente sigue donde creemos que está.
8. Imagen para simulación, registro y localización
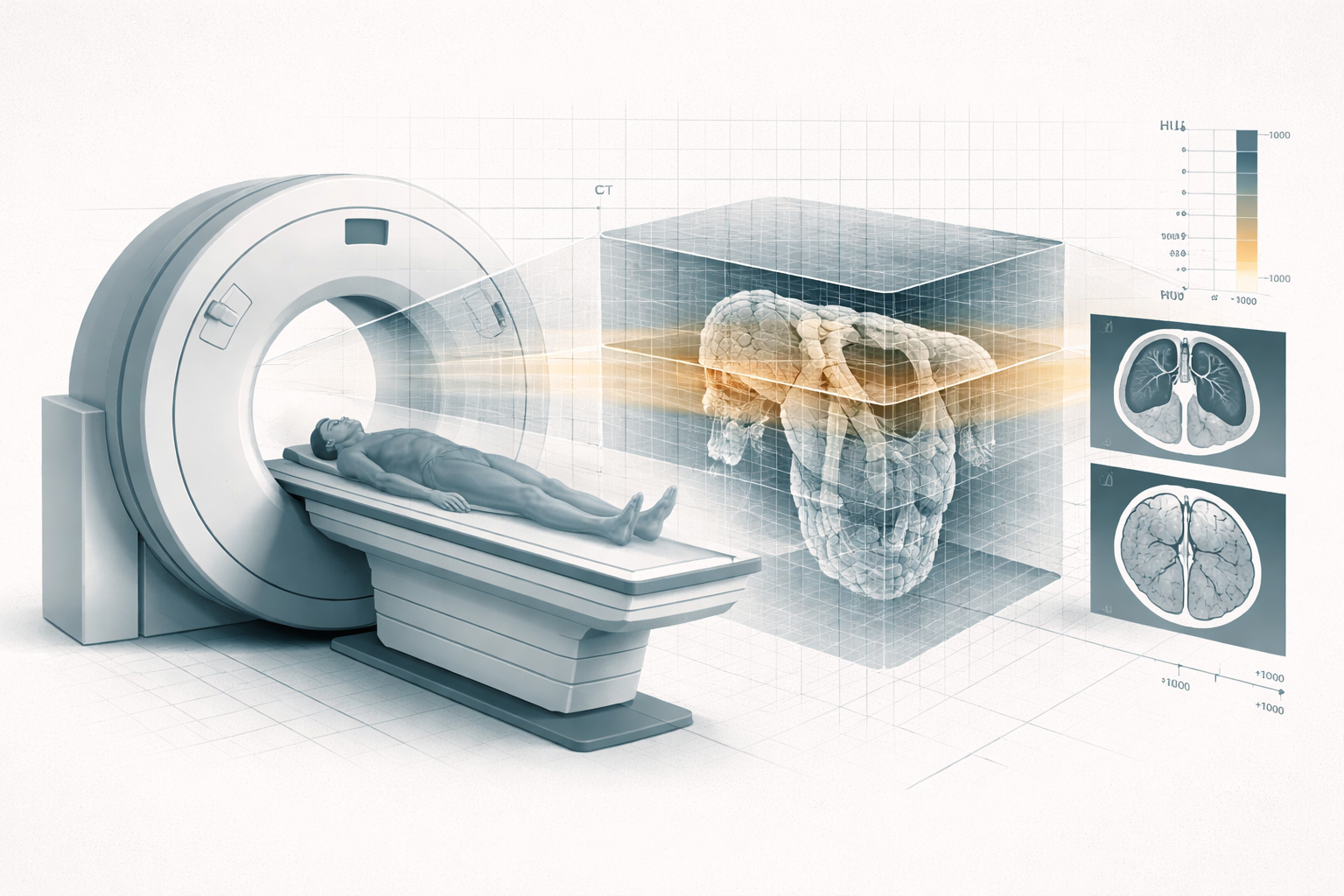
La radioterapia moderna es inseparable de la imagen.
El TAC de simulación sigue siendo la base anatómico-dosimétrica porque aporta geometría consistente y una magnitud física utilizable para cálculo de dosis. Pero muy a menudo no basta solo con TAC.
Aquí entran como complementarias:
- RM, para mejorar tejidos blandos, extensión local y delimitación;
- PET, para incorporar información metabólica o funcional;
- ultrasonidos, en algunos guiados y reconstrucciones geométricas concretas;
- y registros rígidos o deformables para fusionar información de modalidades distintas.
Es necesario separar dos conceptos:
- registro: alinear imágenes entre sí, por ejemplo TAC con RM o PET, para que distintas fuentes de información queden en un mismo marco anatómico;
- localización: colocar al paciente real dentro del sistema de coordenadas de la máquina de tratamiento.
No son lo mismo. El registro ocurre entre datasets. La localización ocurre entre el paciente físico, la mesa, los láseres, la imagen guiada y el isocentro del equipo.
Lo importante es entender que la imagen en radioterapia no es solo diagnóstica. Es también operativa. Sirve para delinear, registrar, localizar, verificar y tratar.
9. Delineación y planificación dosimétrica
Una vez tenemos imagen, empieza una parte especialmente delicada: la delineación.
Hay que contornear:
- volúmenes objetivo;
- órganos de riesgo;
- estructuras auxiliares;
- y, en muchos casos, regiones que condicionan optimización o evaluación.
Después llega la planificación propiamente dicha:
- selección de técnica;
- elección de energías cuando aplica;
- disposición de campos o arcos;
- colimación y modulación;
- cálculo de dosis;
- y optimización iterativa.
Aquí se ve claramente que la planificación no es un dibujo bonito. Es una negociación cuantitativa entre cobertura tumoral y protección tisular.
10. DVH y prescripción
Uno de los objetos más característicos de este mundo es el DVH (Dose-Volume Histogram).
El DVH no sustituye a la distribución espacial completa de dosis, pero permite resumir muy bien cuánto volumen recibe qué dosis. Es una herramienta central para evaluar:
- cobertura del PTV;
- hot spots;
- dosis en OAR;
- compromisos entre planes;
- y adecuación a restricciones clínicas.
La prescripción se expresa habitualmente en Gy (gray), que es la unidad de dosis absorbida. La forma de prescribir depende muchísimo del contexto:
- en fraccionamiento convencional son frecuentes esquemas del orden de 1.8–2 Gy por fracción;
- en hipofraccionamiento las fracciones son mayores;
- en radiocirugía o SBRT pueden usarse pocas fracciones con dosis por fracción mucho más altas.
No debe fijarse como una tabla cerrada porque cambia por tumor, intención, órgano, técnica y tolerancia. Pero sí conviene dejar clara una idea: en radioterapia la pregunta no es solo cuánta dosis total damos, sino cómo la repartimos en el tiempo y en el espacio. Esa distribución es, en el fondo, una negociación entre probabilidad de control tumoral y probabilidad de toxicidad.
11. Localizaciones y movimiento anatómico
No todos los tratamientos se parecen.
Cerebro
El cerebro tiene una ventaja geométrica muy importante: se mueve poco respecto a otras regiones. Eso permite alcanzar precisiones muy altas, márgenes pequeños y técnicas como la radiocirugía con una lógica espacial especialmente fuerte.
Pero esa ventaja viene acompañada de un problema igual de serio: en neuro-radioterapia y radiocirugía se trabaja a menudo muy cerca de estructuras donde un milímetro importa muchísimo.
Ahí están, por ejemplo:
- el quiasma óptico, donde una desviación relevante puede traducirse en pérdida visual grave;
- el tronco cerebral, cuya función es tan básica que basta nombrarla para entender por qué su tolerancia condiciona todo el plan;
- nervios craneales y estructuras funcionales críticas;
- y lesiones próximas a vasos o regiones donde incluso pequeñas variaciones anatómicas o dinámicas pueden tensar al máximo la intervención.
Por ello, el cerebro exige alta precisión geométrica y control estricto de incertidumbres.
Tórax, abdomen y pelvis
Aquí el cuerpo se vuelve mucho menos obediente.
- el pulmón se mueve con la respiración;
- el corazón introduce dinámica propia;
- la vejiga y el recto cambian;
- las asas intestinales se recolocan;
- la próstata puede variar de posición relativa;
- y la anatomía blanda obliga a convivir con incertidumbre real.
Por eso en tejidos blandos y regiones móviles la radioterapia exige más imagen, más verificación, más márgenes o más estrategias de control del movimiento. Aquí el problema no es solo calcular bien. Es tratar lo que creemos estar tratando en el instante real del tratamiento.
12. Radiocirugía: precisión extrema
La radiocirugía merece mención aparte porque concentra muy bien el ideal geométrico de la radioterapia.
No es cirugía en sentido convencional. No abre. No reseca. Pero sí intenta producir un efecto muy localizado mediante haces extremadamente conformados y controlados.
Tiene especial protagonismo en:
- lesiones cerebrales pequeñas;
- malformaciones vasculares seleccionadas;
- algunas lesiones funcionales muy concretas;
- y variantes extracraneales cuando hablamos de SBRT.
Aquí la precisión no es un lujo técnico. Es la condición de posibilidad del tratamiento.
Y esa precisión no vive en un mundo completamente inmóvil. Incluso en escenarios muy controlados aparecen límites físicos y biológicos: pequeñas pulsaciones vasculares, cambios mínimos de presión, microvariaciones de posicionamiento o diferencias entre la imagen de planificación y la anatomía real del momento. En la mayoría de contextos esas variaciones parecen casi despreciables. En radiocirugía compleja, cerca de estructuras críticas, pueden ser exactamente la clase de detalle que obliga a extremar márgenes, verificación y prudencia.
13. Set-up diario, IGRT y verificación
Una de las grandes dificultades reales de la radioterapia no es solo calcular bien un plan, sino trasladar correctamente al paciente desde el espacio de la imagen y la planificación al espacio físico de la máquina.
Ese traslado exige control geométrico. Exige que la posición usada para simular, delinear y optimizar pueda reproducirse después de forma suficientemente fiel en la sala de tratamiento. Ahí aparecen inmovilizadores, marcas, láseres, sistemas de imagen guiada, surface imaging y protocolos de corrección.
El plan requiere una entrega geométricamente consistente.
Eso exige una cadena diaria de comprobación:
- identificación del paciente;
- colocación e inmovilización;
- localización dentro del sistema de coordenadas del equipo;
- centrado;
- imagen guiada cuando aplica;
- correcciones de posicionamiento;
- y verificación de que la geometría del día no traiciona la intención del plan.
Por eso hoy hablamos mucho de IGRT (Image-Guided Radiation Therapy). No porque la imagen sea un extra elegante, sino porque el tratamiento real sucede en días distintos, con anatomías que pueden cambiar y márgenes que a veces son estrechos.
La localización no es una formalidad. Es el paso que convierte una intención geométrica en una entrega física real. Y precisamente por eso el control del paciente durante el traslado entre imagen, planificación y tratamiento es tan importante como el cálculo mismo.
14. Papel del físico médico
En pocas áreas se ve tan claro como aquí.
El físico médico participa en:
- aceptación y puesta en marcha de equipos;
- commissioning;
- validación de algoritmos y sistemas de planificación;
- dosimetría absoluta y relativa;
- control de calidad periódico;
- verificación independiente;
- auditorías;
- revisión de incidencias;
- protección radiológica;
- y soporte técnico-clínico para que el tratamiento planificado sea realmente tratable.
Si esto se hace mal, el problema no es solo técnico. Puede convertirse en un problema clínico severo.
15. Máquinas, fuentes y control físico
Aquí aparece una parte muy de física que merece notarse en un blog como este.
La radioterapia necesita medir y validar constantemente.
Hay que controlar:
- estabilidad del haz;
- simetría y planitud cuando aplica;
- coincidencias geométricas e isocentro;
- rendimiento dosimétrico;
- sistemas de imagen asociados;
- exactitud de colimación;
- y coherencia entre planificador, datos comisionados y máquina real.
En tratamientos con fuentes radiactivas esto añade otra capa: la actividad cambia con el tiempo. El decaimiento radiactivo no es una nota al pie, sino parte del trabajo real. Afecta a calibración, tiempos de tratamiento, trazabilidad y control de calidad.
Eso vale para braquiterapia, para equipos basados en fuentes selladas y para sistemas históricos o especializados donde el comportamiento de la fuente es parte central del procedimiento.
16. Equipamiento y finalidad clínica
La enumeración de equipos no define la disciplina.
Lo que de verdad la define es otra cosa:
- una diana clínica;
- una geometría tratable;
- una dosis prescrita;
- restricciones de órganos sanos;
- una cadena de validación;
- y un sistema humano y técnico capaz de repetir el tratamiento con seguridad.
Las máquinas importan porque sirven a esa arquitectura conceptual y clínica, no al revés.
17. Resumen técnico
La radioterapia materializa la conversión de información anatómica y funcional en una intervención dosimétrica controlada.
Su fiabilidad depende de la coherencia entre imagen, planificación, verificación, entrega y control de calidad. Este sistema exige integración técnica y responsabilidad clínica sostenida.
Relacionado
Para ampliar
- IAEA - Radiotherapy
- IAEA - What is Radiation Therapy?
- IAEA - Medical Physics: Radiotherapy
- IAEA - Radiotherapy Equipment
- NCI - Radiation Therapy for Cancer
- NCI - External Beam Radiation Therapy for Cancer
- AAPM Report No. 46 - Comprehensive QA for Radiation Oncology
- AAPM TG-142 - Quality Assurance of Medical Accelerators
- AAPM TG-302 - Surface Guided Radiotherapy